Почему замерзают аккумуляторы? | АКБ-сервис
Почему замерзают аккумуляторы?
Никто из автолюбителей не застрахован от того, что одним морозным утром он обнаружит тот факт, что в аккумуляторе замерз электролит. Визуально это можно определить по вздувшимся стенкам АКБ, а также по отказу работы абсолютно всех электро систем автомобиля. Так почему же замерзает аккумулятор, эксплуатирующийся сравнительно недолгое время, а подчас даже и совсем новый? Давайте разберемся с физико-химическими процессами, которые протекают внутри аккумулятора.
При разряде аккумулятора в процессе электролитической диссоциации серная кислота воздействует на свинец в пластинах и в результате этого активно образуются углекислый газ, сульфат аммония и вода. Замерзанию как раз таки подвержена вода в аккумуляторе и чем ниже будет плотность электролита, тем выше температура замерзания. Следовательно, делаем вывод, что если ваш аккумулятор замерз, то он был разряжен, либо электролит имел малую плотность по другим причинам.
Иногда такие простые, казалось бы, причины, как ослабление или окисление контактов соединения с электропроводкой, приводят к снижению эффективности зарядки от генератора из-за падения напряжения на клеммах аккумулятора, при этом сам аккумулятор абсолютно исправен, но систематически недозаряжается. Прибавьте к этому низкую температуры за бортом автомобиля и получите результат – аккумулятор не принимает заряд.
Этому явлению есть довольно простое объяснение. При низких температурах в аккумуляторах повышается вязкость электролита, скорость протекания электрохимических реакций замедляется, и в итоге снижается способность аккумулятора быстро заряжаться.
В таких случаях автомобилисты вынуждены эксплуатировать свои аккумуляторы в состоянии неполного заряда и, естественно, с более низкой ёмкостью. При каждом последующем пуске аккумулятор, как правило, недопустимо глубоко разряжается, а зарядиться быстро до требуемой ёмкости и напряжения уже не может.
Конечно, электролит замерзнуть не может, а вот когда весь ресурс аккумулятора исчерпан и вся серная кислота израсходована на процессы разрядки, то в электролите остается практически одна вода, температура которой составляет 0 С.
Еще очень часто распространено такое явление, как утечка тока в цепи — обычно это может быть магнитола, сигнализация или другое не штатное оборудование, подключенное не правильно. Даже видеорегистратор если хотите. Он буквально за сутки разрядит АКБ и тот даже при малых морозах – замерзнет! Драгоценные амперы могут также расходоваться из-за попадания влаги, или перетертой проводки- иногда причину бывает сложно найти. Или же внезапная неисправность в генераторе — вышедший из строя регулятор напряжения или диодный мост, также могут быть причиной быстрой разрядки аккумулятора, и следовательно замерзания электролита в мороз.
Ниже приведены температуры замерзания электролита в аккумуляторе при разряде:
Вода при замерзании увеличивается в объеме и выдавливает активную массу из ячеек решетки, в результате мы имеем снижение по токотдаче и сроку службы. Такой аккумулятор теряет свой ресурс и, как правило, преждевременно выходит из строя. Именно поэтому величина тока холодной прокрутки и запас ёмкости в аккумуляторе в холодное время года имеет такое большое значение для беспроблемной эксплуатации.
Такой аккумулятор теряет свой ресурс и, как правило, преждевременно выходит из строя. Именно поэтому величина тока холодной прокрутки и запас ёмкости в аккумуляторе в холодное время года имеет такое большое значение для беспроблемной эксплуатации.
Что делать с замерзшим АКБ? Как правильно разморозить и зарядить замерзший аккумулятор?
Первым делом нужно убедиться в дальнейшей пригодности батареи путем осмотра корпуса на предмет трещин и разломов (очень часто лед внутри разрывает тонкие пластиковые стенки корпуса). После осмотра аккумуляторную батарею следует снять с автомобиля и поставить в теплое помещение.
Самое главное не заряжать аккумулятор пока в нем находиться лед, чтобы избежать замыкания.
Батарея должна оттаять полностью и температура электролита должна приблизиться к комнатной. После размораживания мы еще раз осматриваем нет ли течей по корпусу (вздувшиеся стенки должны принять исходный вид). Если на корпусе аккумулятора вы наблюдаете какую-то жидкость, то следует определить ее происхождения с помощью лакмусового индикатора.
Иногда случается так, что мелкие трещины на корпусе аккумулятора оставляют без внимания, принимая слегка влажные стенки за водный конденсат. В итоге после того как АКБ будет разморожен, заряжен и готов к эксплуатации, он будет медленно, но уверено течь. Есть конечно вариант запайки корпуса аккумулятора ( для этого сливаем все содержимое и берем паяльник в руки ), но вероятность положительного исхода этой операции примерно один к десяти. Потому что
Далее приступаем к зарядке, помня о том, что ток заряда определяем как десять процентов от номинальной емкости аккумулятора в ампер/часах. В таком случае процесс зарядки длиться около десяти часов. Но, это «кустарный метод». В идеале зарядка батареи производиться разным током, изначально нужно пробить сульфатацию на пластинах АКБ импульсным высоким током, потом постоянным пониженным дать основную зарядку и доводить батарею на прерывающемся низком току для полного восстановления пластин. Главное – мы должны зарядить батарею полностью (желательно автоматическим зарядным устройством), после этого обязательно проверяем прозрачность и плотность электролита. Мутный электролит свидетельствует о том, что пластины осыпались. Если все в порядке, то можно спокойно ставить АКБ и ездить дальше.
В таком случае процесс зарядки длиться около десяти часов. Но, это «кустарный метод». В идеале зарядка батареи производиться разным током, изначально нужно пробить сульфатацию на пластинах АКБ импульсным высоким током, потом постоянным пониженным дать основную зарядку и доводить батарею на прерывающемся низком току для полного восстановления пластин. Главное – мы должны зарядить батарею полностью (желательно автоматическим зарядным устройством), после этого обязательно проверяем прозрачность и плотность электролита. Мутный электролит свидетельствует о том, что пластины осыпались. Если все в порядке, то можно спокойно ставить АКБ и ездить дальше.
Как не допустить того чтобы в аккумуляторе замер электролит?
Основная задача, которая стоит перед водителем, по уходу за АКБ – это не допускать его разряда или перезаряда.
Это же касается и вопроса замерзания батареи. В большинстве случаев замерзает разряженный аккумулятор. Так же важно постоянно следить за плотностью электролита, проверку плотности производим в каждой отдельной банке.
Краткий вывод: замерзание батареи – это еще не ее конец. С аккумулятором нужно быть особо внимательным в зимнюю пору. Заряженная батарея с нормальной плотностью электролита – не замерзает!
Проверяем и восполняем уровень электролита в аккумуляторе. Сколько электролита должно быть в аккумуляторе? Какой уровень воды в аккумуляторе
От качества электролита сильно зависит долговечность и основные параметры аккумулятора. Поэтому если вы хотите, чтобы батарея служила вам верой и правдой не один год, предлагаем ознакомиться с основными нюансами ее обслуживания.
1 Почему электролит важен для аккумулятора?
Электролит – это раствор серной кислоты (Н2SO4) в воде, который способен накапливать и раздавать электрическую энергию в результате происходящих в нем химических реакций. Крайне важно, чтобы уровень этого раствора в (АКБ) находился в пределах нормы. Дело в том, что излишек жидкости приводит к окислению клемм, а это может стать причиной выхода из строя всей бортовой электроники.
Если же уровень электролита меньше положенной нормы, происходит пересыхание внутренних пластин и повышение плотности кислоты. В результате пластины начинают разрушаться, и АКБ окончательно выходит из строя. В таких случаях говорят: «В аккумуляторе «посыпались банки». Поэтому в интересах каждого автовладельца следить за уровнем электролита и поддерживать его на определенном уровне.
2 Проверка количества электролита в батарее
Аккумулятор, казалось бы, представляет собой замкнутую емкость, поэтому уровень жидкости в ней не должен изменяться. На практике же в процессе эксплуатации АКБ вода испаряется. Причем скорость уменьшения жидкости зависит от нескольких моментов:
На практике же в процессе эксплуатации АКБ вода испаряется. Причем скорость уменьшения жидкости зависит от нескольких моментов:
- условий эксплуатации авто – перепады температур, часто включение и выключение зажигания, длительные поездки по трассе приводят к ускоренному испарению воды;
- исправности электрической системы – если имеются проблемы с электрикой, увеличивается нагрузка на АКБ. Особенно негативно на состоянии батареи сказываются проблемы с генератором.
На аккумулятор оказывает влияние и манера вождения автомобиля, и некоторые другие факторы. При их сочетании уровень жидкости может упасть до критического в течение одного месяца. Но как его контролировать?
Проверка уровня может быть выполнена несколькими способами. Чаще всего корпус АКБ выполняют из полупрозрачного пластика и наносят метки «Min» и «Max». Соответственно, уровень раствора хорошо виден на глаз, особенно если поднять аккумулятор перед собой в солнечный день или в хорошо освещенном помещении.
Если пластик не просвечивается или на батарее отсутствуют метки, проверить уровень можно при помощи стеклянной трубки. Для этого нужно открутить пробку аккумулятора, затем опустить трубку до упора и закрыть верхнее отверстие пальцем. После этого надо вытащить трубку и замерить высоту столбика жидкости. Минимально допустимое значение составляет 12 мм, а максимальное – 15 мм. Подобным образом необходимо проверить уровень жидкости в каждой банке.
В современных дорогих моделях АКБ имеется специальный датчик уровня жидкости, так называемый «магический глаз». Чтобы проверить уровень, нужно аккуратно по нему постучать, после чего проявится определенный цвет. Каждый цвет имеет свое значение:
- зеленый – аккумулятор в норме;
- белый – уровень заряда меньше нормы, т.е. батарею нужно зарядить;
- красный – необходимо долить жидкость.
Надо сказать, что «магический глаз» не точно диагностирует состояние АКБ, поэтому желательно произвести дополнительную проверку.
3 Корректируем количество электролита
Если проверка показала, что уровень жидкости в банках низкий, его необходимо увеличить, путем доливки воды. Имейте в виду, что в аккумулятор можно заливать исключительно дистиллированную воду. Если вы зальете воду из-под крана, то АКБ разрядится полностью или вообще выйдет из строя, так как кислота вступит в реакцию с компонентами, которые имеются в водопроводной воде.
Температура дистиллированной воды, доливаемой в банку, должна быть в пределах 15-25 градусов.
Если уровень кислотного раствора превышает норму, его необходимо откачать. Для этих целей можно использовать шприц или спринцовку. После доливки жидкости желательно замерить уровень заряда. Если заряд низкий, АКБ нужно поставить заряжаться в течение нескольких часов.
4 Что еще нужно знать об электролите?
Важным параметром электролита является его плотность. Серная кислота сама по себе достаточно плотное вещество – этот параметр составляет 1,84 г/см³. Что касается плотности водяного раствора в аккумуляторе, показатель должен находиться в пределах 1,27–1,28 г/см³. Если плотность электролита в аккумуляторе будет отличаться от положенной, долговечность АКБ сильно снизится и изменятся основные параметры.
Что касается плотности водяного раствора в аккумуляторе, показатель должен находиться в пределах 1,27–1,28 г/см³. Если плотность электролита в аккумуляторе будет отличаться от положенной, долговечность АКБ сильно снизится и изменятся основные параметры.
Среди автомобилистов «советской закалки» бытуем мнение, что зимой плотность электролита должна быть выше, чем летом. В действительности же в современные аккумуляторы и зимой, и летом заливают кислотный раствор плотностью 1,27 г/см³. При такой плотности жидкость начинает замерзать при температуре -60 градусов.
Для проверки плотности применяют специальный прибор, который называется ареометром. Он представляет собой стеклянную трубку со шкалой, внутри которой расположен поплавок. С одной стороны трубки расположена резиновая груша, которая позволяет набирать в трубку жидкость. После забора электролита поплавок свободно перемещается вдоль трубки и показывает уровень плотности.
При проверке плотности соблюдайте два правила:
- после доливки дистиллированной воды нельзя сразу проверять плотность.
 Должно пройти некоторое время, чтобы вода хорошо перемешалась с водой. Обычно для этого требуется 3-4 часа;
Должно пройти некоторое время, чтобы вода хорошо перемешалась с водой. Обычно для этого требуется 3-4 часа; - измеряйте и корректируйте плотность после полной зарядки АКБ.
Если ареометр показал, что плотность слишком низкая, следует долить специальный корректирующий электролит, плотность которого составляет 1,4 г/см³. Корректирующий электролит можно купить или сделать самостоятельно, смешав серную кислоту с дистиллированной водой. Единственное, работайте с кислотой очень осторожно, соблюдая все правила техники безопасности. Причем заниматься этим лучше на улице, но не в домашних условиях. Учтите, что в процессе смешивания кислоты с дистиллированной водой выделяется тепло.
Ни в коем случае не заливайте серную кислоту прямо в аккумулятор, так как жидкость может закипеть и АКБ выйдет из строя.
Если оказалось, что плотность электролита выше положенного значения, слейте с банок небольшое количество раствора в специальную емкость и добавьте дистиллированную воду. Так как концентрация серной кислоты в электролите достаточно высокая, работать с жидкостью необходимо тоже очень осторожно.
Так как концентрация серной кислоты в электролите достаточно высокая, работать с жидкостью необходимо тоже очень осторожно.
5 Восстанавливаем старый аккумулятор новым электролитом
Если вы заметили, что АКБ стал быстро разряжаться, при этом электрика в автомобиле в полном порядке, скорее всего батарея выходит из строя. Но не спешите отправляться в автомагазин за покупкой нового аккумулятора. Как правило, замена раствора позволяет исправить ситуацию.
Надо сказать, что заменить электролит имеет смысл и в других некоторых случаях:
- АКБ длительное время не использовался;
- жидкость стала мутной. Имейте в виду, что серый оттенок раствора может свидетельствовать о том, что АКБ нужно зарядить. После полноценной зарядки первоначальная прозрачность жидкости возвращается.
Прежде чем поменять жидкость, подкорректируйте плотность нового электролита, чтобы она составляла 1,28 г/см³. Старый кислотный раствор полностью слейте и залейте дистиллированную воду. Затем аккумулятор нужно интенсивно потрясти и слить с него воду. Повторяйте процедуру до тех пор, пока вместе с водой не выйдет вся угольная крошка.
Затем аккумулятор нужно интенсивно потрясти и слить с него воду. Повторяйте процедуру до тех пор, пока вместе с водой не выйдет вся угольная крошка.
Перед заливкой в электролит желательно добавить специальную присадку, удаляющую сульфат с электродов. Затем залейте жидкость в горловины банок. Делайте это потихоньку, при помощи воронки с узким горлышком. Чтобы присадка полностью растворилась, аккумулятор нужно оставить на 48 часов. После этого необходимо поставить его на зарядку под током 0,1 А. Зарядка должна осуществляться циклично, т.е. по схеме зарядка/разрядка, пока не восстановится плотность электролита. В итоге напряжение на клеммах должно составлять 14-15 В.
По достижении этого напряжения зарядный ток следует уменьшить в два раза и заряжать батарею еще на протяжении двух часов. Если плотность не меняется, зарядку надо прекратить и разрядить АКБ до напряжения 10 В с применением тока 0,5 А.
- T – время разрядки;
- I – разрядный ток;
- С – емкость АКБ.

Если оказалось, что емкость составляет менее 4 ампер/часов, цикл заряда необходимо повторить, чтобы повысить показатель емкости. Если вы произведете вышеописанную процедуру правильно, о покупке нового аккумулятора на некоторое время можно будет забыть.
Очень важно не только уметь хорошо управлять автомобилем, но и знать, из чего состоит машина, как за ней следить и правильно ее обслуживать. В этой статье рассмотрим актуальный вопрос для АКБ: каким должен быть уровень электролита в автомобильном аккумуляторе, и на что он влияет?
Электролит и его роль в аккумуляторе
Итак, начнем с определения, что же все-таки называется электролитом. Это попросту раствор серной кислоты и дистиллированной воды. Причем наличие каких-то посторонних примесей недопустимо, ведь тогда изменится его плотность, что самым негативным образом отразится на работе аккумуляторной батареи. Также очень важную роль играет и его уровень. Так, например, если он будет ниже нормы, произойдет высыхание внутренних пластинок и мощность снизится.
Не стоит думать, что выходом будет доливание жидкости сверх нормы, ведь в этом случае кислота разъест внешнюю часть агрегата. Кроме того, можно столкнуться и с такими проблемами, как быстрая саморазрядка батареи или выход из строя регулятора напряжения. В общем, залогом нормального функционирования вашего автомобиля служит надлежащий уровень электролита, поэтому периодически следует осматривать АКБ.
Как проверить уровень электролита в аккумуляторе?
Бытует мнение, что аккумуляторные батареи не нуждаются в техническом обслуживании, и, в принципе, так оно и есть, но учтите — речь идет о нормальных условиях эксплуатации. Любителям же путешествовать на своем «железном коне» или же жителям регионов, в которых царит очень жаркое лето, все-таки стоит контролировать вышеуказанный параметр. Ведь в состав электролита входит вода, а она, как известно, имеет свойство испаряться.
Кроме того, интенсивному выкипанию способствуют и неисправности реле-регулятора. О том, что пора проверить состояние аккумулятора, свидетельствуют следующие признаки:
- из заливных отверстий сильно парит;
- на корпусе АКБ можно увидеть капли электролита;
- сам аккумулятор очень интенсивно нагревается.

Проверка уровня электролита в аккумуляторе осуществляется разными способами. Наиболее простой – визуальный контроль. Обычно корпус батареи, в котором находится жидкость, делают прозрачным, и на него наносятся отметки, указывающие максимальный и минимальный уровень. И, соответственно, количество электролита должно находиться в этих пределах.
Снижается уровень электролита за счет испарения воды или вытекания состава из-за повреждения корпуса. В первом случае можно самостоятельно поправить состояние АКБ.
Но иногда такая возможность отсутствует, тогда необходимо действовать примерно так. Берем прозрачную трубочку диаметром в 5 миллиметров и опускаем ее в резервуар до упора. Затем плотно зажимаем пальцем наружное отверстие трубки и вытаскиваем ее. В ней будет находиться измеряемая жидкость. Уровень электролита будет соответствовать высоте его столба в данной трубочке.
В АКБ низкий уровень электролита – что делать автовладельцу?
Итак, высота жидкости в трубке должна быть в пределах 10–15 миллиметров. Если ее больше нормы, тогда следует убрать лишнюю. Сделать это довольно просто, нужна всего лишь резиновая груша или шприц, которыми за считаные секунды можно выкачать излишки. Естественно, после этой операции еще раз осуществляем проверку. А вот если анализ показал низкий уровень электролита, что делать тогда?
Если ее больше нормы, тогда следует убрать лишнюю. Сделать это довольно просто, нужна всего лишь резиновая груша или шприц, которыми за считаные секунды можно выкачать излишки. Естественно, после этой операции еще раз осуществляем проверку. А вот если анализ показал низкий уровень электролита, что делать тогда?
В таком случае заливать новый раствор не рекомендуется, так как это повлияет на плотность и также негативно отразится на состоянии батареи . Ведь испаряется только вода, а концентрация серной кислоты остается прежней. Поэтому следует добавлять дистиллированную воду комнатной температуры. Причем использование простой жидкости из крана категорически запрещено, так как батарея может разрядиться. Заливать сам электролит можно только в одном случае: если его уровень снизился из-за разбрызгивания либо вытекания.
Уровень электролита в аккумуляторе – это то, на что должен обращать внимание каждый автомобилист. Ведь от данного параметра зависит работоспособность автотранспорта, срок эксплуатации и частота обслуживания акб. Допустимо выполнение таких действий в домашних условиях.
Допустимо выполнение таких действий в домашних условиях.
Автомобили комплектуются такими аккумуляторами:
- WET (свинцово-кислотные акб). Электролит представлен в виде водного раствора, включающего серную кислоту.
- AGM. Отличаются тем, что входящее в состав стекловолокно пропитано электролитическим составом.
- GEL (гелиевый акб). Электролит представлен в виде геля. Для этого в серно-водный раствор введена окись кремния.
Определять, сколько электролита в аккумуляторе, необходимо, если речь идет о свинцово-кислотных источниках питания.
Особенности проверки уровня электролита в автомобильном аккумуляторе
Регулярно проверяя уровень электролита в аккумуляторе, контролируя плотность, можно поддерживать автотранспорт, отдельные узлы в работоспособном состоянии. При необходимости проводят корректировку плотности, увеличивают или уменьшают уровень электролитического состава. Ведь использование источника питания, в котором электролитической жидкости меньше нормы, приводит к пагубным последствиям.
Просмотрите интересное видео про уровень электролита.
Проверка уровня электролита
Информация о том, какой уровень электролита должен быть, присутствует в технической документации, которая прилагается к автотранспортному средству. Для проверки и контроля используется два метода, каждый из которых имеет свои особенности:
- На корпусе АКБ сосредоточены отметки max и min. Если корпус подготовлен из прозрачного материала, то легко определить количество электролитического состава. На основании полученной информации нужно принимать решение об уменьшении, увеличении дистиллированной воды. Такой способ малоэффективен, если корпус окрашен в черный цвет.
- Уровень электролита в акб проверяют с помощью стеклянной, пластиковой трубочки. Диаметр трубки – 3–5 мм. Перед тем как ввести трубку, изымается пробка. Опускается трубка до момента соприкосновения с пластинами. Норма – 12 мм. Такая процедура проводится для каждой банки, входящей в состав аккумуляторной батареи.

Избыток электролитического состава изымается с помощью шприца. Этот же инструмент используется для введения подготовленного электролита или дистиллированной воды.
Для того чтобы определить уровень жидкости в необслуживаемых источниках питания, используются отметки на поверхности акб. Дополнительно применяется индикатор заряда.
Причины снижения уровня электролита
- Чрезмерное увеличение выдаваемого генератором напряжения.
- Деформация корпуса аккумуляторной батареи, появление микротрещин или других дефектов.
- КЗ внутри источника питания.
- Наличие свинцового осадка и мусора.
В кислотно-свинцовых источниках питания уровень дистиллята постепенно снижается. При этом неопытные автомобилисты пытаются исправить ситуацию, добавив водный раствор с введенной серной кислотой. В результате, увеличивается уровень и плотность. Это приводит к тому, что аккумуляторная батарея быстро выходит из строя, внутренняя часть стремительно разрушается.
Неправильно определенный уровень приводит к таким последствиям:
- Разрушение свинцовых пластин, формирование остатков и шлама.
- Со временем образуются мостики между включенными в состав пластинами. Такие мостики способствуют возникновению КЗ, снижению мощности.
- Появление подтеков, затрудняющих эксплуатацию аккумуляторной батареи.
- Окисление основных контактов.
- Выход из строя аккумуляторной батареи.
Определение плотности электролитического состава
К проверке плотности приступают после тщательной зарядки аккумуляторной батареи. Предварительно подготавливается прибор, при помощи которого устанавливается степень плотности. Чаще всего используется ареометр.
С банок, сосредоточенных в корпусе источника питания, изымаются пробки. В отверстие помещается ареометр, набирается немного электролитического состава. Поплавок, включенный в состав, содержит шкалу с соответствующими отметками, которая используется для определения степени плотности. Оптимальный показатель – 1,29-1,3 г/см3.
Оптимальный показатель – 1,29-1,3 г/см3.
Для понижения степени плотности электролитического состава допускается применение дистиллята, который реализуется в специальных магазинах, аптеках. Процедура введения дистиллированной воды осуществляется поэтапно. При этом в каждой банке периодически измеряется этот показатель.
Повысить плотность сложнее, чем увеличить уровень электролита в акб. Ведь изначально изымается часть состава при помощи ареометра, другого инструмента. После этого вводится смесь с соответствующей плотностью. Иногда возникает потребность в полной замене жидкости. Выявить это можно, если знать, как проверить уровень, степень плотности.
Процедура замены электролита
Полную замену проводят при условии, что уровень плотности значительно снизился. Процедура имеет особенности, правила. Перед выполнением нужно подготовить:
- Смесь с соответствующей плотностью (около 1,29 г/см3).
- Тара, подходящая для размещения старого раствора.
- Ареометр или другой инструмент.

Запрещено переворачивать источник питания для последующего удаления водно-серного раствора. Ведь это приводит к разрушению свинцовых пластин, образованию мостиков и подтеков, замыканию.
Перед работой должно быть подготовлено все необходимое для защиты: перчатки из плотной резины, прочная одежда, защитные очки. Ведь попадание смеси на кожу провоцирует образование химических ожогов.
Для откачки старой смеси применяют «грушу» или другой инструмент. Откачиваемую жидкость помещают в специальную тару, отличающуюся стойкостью, прочностью.
Заливку новой смеси выполняют поэтапно, соблюдая правила, нормы.
Меры безопасности
При работе с растворами, в состав которых входит серная кислота, требуется выполнение таких правил:
- Все предметы одежды, элементы должны быть подготовлены из прочности и стойкого материала.
- Для хранения использованной электролитической смеси применяется стеклянная либо полиэтиленовая тара, оснащенная плотными крышками и оплеткой.

- Для заливки используется только качественный состав, реализуемый в специальных магазинах. Самостоятельная подготовка приемлема при условии, что человек обладает требуемым опытом и знаниями, инструментами.
- Замена электролитической смеси проводится только после отключения аккумуляторной батареи, ее демонтажа.
- Перед подключением источника питания проверяется состояние выводов, ликвидируются окислы.
Точно определить уровень, плотность электролитического состава несложно. Достаточно соблюдать правила и рекомендации, подготовленные специалистами. С особой тщательностью нужно выбирать помещение, в котором будут проводиться все работы. В помещении должна быть вентиляционная система. Ведь в смеси присутствует кислота, другие вещества.
Своевременная проверка основных показателей – залог эффективной работы аккумуляторной батареи.
Видео про проверку электролита в аккумуляторе
От состояния аккумулятора зависит, сможете вы завести мотор своего автомобиля, или нет. Прочитав статью, вы узнаете, что влияет на уровень электролита и научитесь определять и регулировать его. Вы узнаете, как уровень электролита влияет на состояние аккумулятора и почему падение уровня снижает не только емкость, но и ресурс аккумуляторной батареи.
Прочитав статью, вы узнаете, что влияет на уровень электролита и научитесь определять и регулировать его. Вы узнаете, как уровень электролита влияет на состояние аккумулятора и почему падение уровня снижает не только емкость, но и ресурс аккумуляторной батареи.
Что влияет на уровень электролита
Для ответа на этот вопрос, необходимо понимать, что происходит внутри аккумулятора во время заряда и разряда. При подаче зарядного тока диоксид свинца на катоде (отрицательном контакте) отдает не только свободные электроны, но и молекулы кислорода, превращаясь в свинец. На аноде (положительном электроде) наоборот, свинец впитывает из электролита электроны и молекулы кислорода, превращаясь в диоксид свинца. В обоих процессах из электролита выделяется свободный водород и незначительное количество кислорода, которые уходят в атмосферу. Чем сильней зарядный или разрядный ток, тем больше водорода и кислорода уходит в атмосферу. Помимо этого сильный зарядный или разрядный ток приводит к закипанию электролита, в результате чего в атмосферу уходит не только чистый водород и кислород, но и водяной пар. Все это со временем приводит к падению уровня электролита. Этот процесс происходит в любом аккумуляторе.
Все это со временем приводит к падению уровня электролита. Этот процесс происходит в любом аккумуляторе.
Почему снижается уровень
Если уровень электролита падает настолько, что открывает свинцовые пластины, то ресурс аккумулятора резко снижается. Это вызвано тем, что в реакции окисления и восстановления вмешивается газообразный кислород из атмосферы. В результате баланс чистого свинца и его диоксида меняется, а вместе с ним падает емкость и рабочее напряжение аккумулятора. Добавление дистиллированной воды позволяет , но не может восстановить их состояние. Еще одна причина, по которой может падать уровень электролита — механическое повреждение корпуса. Даже небольшая трещина, которую очень сложно заметить невооруженным взглядом, может стать причиной потери электролита. При утечке в размере 1 капли в час, за месяц аккумулятор потеряет 30-50 миллилитров электролита. Примерно 0,5 литра в течение года, то есть почти весь электролит одной банки аккумулятора.
Как проверить и восстановить уровень электролита
Для проверки электролита вам понадобятся:
- чистая тряпка, чтобы очистить его поверхность от грязи;
- широкая (не менее 1 см) плоская отвертка, с помощью которой вы будете откручивать заливные пробки;
- фонарик.

Откройте капот и осмотрите аккумулятор. На некоторых автомобилях для проверки и доливки электролита приходится снимать аккумулятор. Если ничто не мешает выкручивать пробки и пользоваться фонариком, то тряпкой очистите аккумулятор от пыли, грязи и капелек жидкости. Его поверхность должна быть сухой и чистой. Если заливные пробки закрыты пластиковой накладкой, то снимите ее. Затем выкрутите все пробки и уберите их в сторону. Уровень электролита должен быть на 1,5-2 см ниже поверхности аккумулятора. Для более точной проверки уровня необходима стеклянная или пластиковая палочка. Вставьте ее в заливное отверстие и доведите до верхнего края пластин. Уровень электролита должен превышать пластины на 1,5-2 см. Если уровень ниже и, вы не видите электролит, посветите в заливное отверстие фонариком. Если видны пластины, значит, ресурс аккумулятора уже пострадал. Если восстановить уровень и плотность электролита, то он будет давать нормальный ток, но емкость снизится.
Если уровень электролита меньше, чем должен быть, проверьте его с помощью ареометра, который можно купить в любом автомагазине. Если плотность электролита разряженного аккумулятора ниже 1,2 г/см³, а полностью заряженного ниже 1,29 г/см³, проблема в корпусе аккумулятора. Испарение кислорода и водорода уменьшает объем, но повышает плотность электролита выше стандартной. Утечка не только снижает объем, но и . Аккумулятор, который теряет электролит чинить бесполезно, в большинстве случаев трещина незаметна. Иначе вокруг аккумулятора было бы мокрое пятно.
Если плотность электролита разряженного аккумулятора ниже 1,2 г/см³, а полностью заряженного ниже 1,29 г/см³, проблема в корпусе аккумулятора. Испарение кислорода и водорода уменьшает объем, но повышает плотность электролита выше стандартной. Утечка не только снижает объем, но и . Аккумулятор, который теряет электролит чинить бесполезно, в большинстве случаев трещина незаметна. Иначе вокруг аккумулятора было бы мокрое пятно.
Убедившись, что проблема не в утечке электролита, приступайте в восстановлению его уровня. Для этого используйте только дистиллированную воду. Желательно наливать ее с помощью лейки. Это позволит избежать разлива воды по поверхности аккумулятора и попадания в банки различных загрязняющих веществ, которые станут участниками химических реакций. Заливайте воду тонкой струйкой, это позволит избежать превышения уровня. Подняв уровень электролита, прочистите отверстие (сапун) пробки и вкрутите ее в аккумулятор. Так поступите с каждой банкой аккумулятора.
Иногда владельцы автомобилей спрашивают о том, как проверить . Если выражаться корректнее и точнее, речь идет о том, как проверить плотность электролита в аккумуляторе. Как известно, уровень электролита в батарее измеряется в том случае, если АКБ относится к категории обслуживаемых. Для того чтобы научиться делать это самостоятельно, как в гараже, так и в домашних условиях, нужно знать о том, что представляет из себя жидкий электролит и как устроена внутри обслуживаемая автомобильная батарея.
Если выражаться корректнее и точнее, речь идет о том, как проверить плотность электролита в аккумуляторе. Как известно, уровень электролита в батарее измеряется в том случае, если АКБ относится к категории обслуживаемых. Для того чтобы научиться делать это самостоятельно, как в гараже, так и в домашних условиях, нужно знать о том, что представляет из себя жидкий электролит и как устроена внутри обслуживаемая автомобильная батарея.
Что находится внутри АКБ
Внутри аккумуляторной батареи автомобиля в определенной последовательности расположены шесть отсеков, или «банок». Каждый отсек имеет свинцовые пластины с положительными и отрицательными зарядами. «Банка» устроена герметично, и ее контакт с другими элементами происходит через общее полярное соединение.
Уровень напряжения в каждом отсеке АКБ составляет 2, максимум — 2,1 вольт. Все элементы соединяются друг с другом в последовательную электрохимическую цепь, имея на выходе общее напряжение 12 вольт.
Благодаря тому, что каждая «банка» заполнена особым химическим соединением, имеющим жидкую консистенцию, автомобильный аккумулятор обладает способностью накопления и отдачи электрического заряда. Эта жидкость получила название «электролит», а такие простые теоретические знания из области физики и химии помогут разобраться в том, как проверить плотность аккумулятора (точнее, электролита) правильно.
Эта жидкость получила название «электролит», а такие простые теоретические знания из области физики и химии помогут разобраться в том, как проверить плотность аккумулятора (точнее, электролита) правильно.
Для чего необходимо проверять плотность электролитической жидкости
Любой электролит представляет собой не что иное, как химическую смесь, состоящую из дистиллированной воды и серной в определенной пропорции: вода 65%, 35% — кислота. Именно такое процентное соотношение и позволяет электролиту осуществлять накопление электрического заряда без нанесения урона чувствительным свинцовым пластинам АКБ.
В процессе постоянной эксплуатации батареи происходят постоянные изменения плотности электролита, что определенным образом может сказаться на ее рабочих функциях. Само понятие плотности, кстати, означает не что иное, как процентное соотношение серной кислоты к дистилляту.
Если уровень серной кислоты внутри аккумулятора становится слишком высоким, это может печально закончиться для его пластин. Бывают ситуации, когда кислота попросту разъедает свинец, и пластины разрушаются.
Бывают ситуации, когда кислота попросту разъедает свинец, и пластины разрушаются.
Если же кислоты слишком мало, это означает, что АКБ разряжена или близка к тому, чтобы разрядиться полностью. Аккумулятор не может работать в режиме той емкости, которая указана в его технических характеристиках. Например, энергии может просто не хватить в условиях холодного запуска двигателя внутреннего сгорания.
Также, если водитель долго пытается ездить на разряженном аккумуляторе, процесс оседания сульфатов на пластинах неизбежен. На них образуется плотный белый налет, убрать который порой бывает весьма проблематично. При критичном уровне сульфатов произойдет либо разрушение пластин, либо короткое замыкание. Потребуется .
Принцип работы аккумуляторной батареи
Чтобы знать, как правильно измерять уровень электролита, важно помнить — любая АКБ работает по цикличному принципу. Вначале она осуществляет накопление заряда внутри, а затем, при запуске двигателя, начинает его постепенно отдавать автомобилю, приводя его в движение. При отдаче заряда аккумулятором кислота выделяет те самые сульфаты (соли), оседающие на пластины «банок». А в «банках» происходит образование воды. Это приводит к тому, что уровень электролита значительно снижается.
При отдаче заряда аккумулятором кислота выделяет те самые сульфаты (соли), оседающие на пластины «банок». А в «банках» происходит образование воды. Это приводит к тому, что уровень электролита значительно снижается.
Что потребуется сделать в данном случае:
- когда уровень плотности выше требуемого, нужно разбавить электролит дистиллированной водой;
- когда плотность снижается, батарея срочно нуждается в полноценной зарядке в течение, как минимум, 10-12 часов.
Как проверить электролит и измерить его плотность
Перед тем как проверить электролит в аккумуляторе, очистите его поверхность от грязи и пыли, чтобы при снятии крышек с батарейных отсеков они не попали внутрь . Возьмите тонкую трубку из стекла, ее диаметр может составлять от 4 до 5 миллиметров. Теперь нужно опустить трубку в отсек до конца, так, чтобы она коснулась его дна. Отверстие можно закрыть с помощью пальца (предварительно не забудьте обезопасить себя, надев технические перчатки!).
Достаньте из банки трубку: в нее должно попасть небольшое количество электролитической жидкости. Ориентируйтесь на ее высоту — сколько места она занимает в трубке. Если высота жидкости 10-15 миллиметров — плотность в пределах нормы, а когда уровень больше, либо меньше — плотность необходимо откорректировать.
Перед тем как приступить к корректировке плотности, нужно произвести ее точные замеры — в каждом аккумуляторном отсеке по отдельности, так как они между собой не сообщаются. Обязательно зарядите АКБ перед измерением, иначе результаты могут оказаться неверными. Кроме этого, незадолго до процесса батарею нужно на 3-4 часа оставить в помещении с комнатной температурой (от 20°С, можно чуть выше). Ведь химическая жидкость имеет прямую зависимость от температурного фактора.
Для измерения уровня плотности электролита применяется такой простой инструмент, как . Его еще иногда называют более сложным словом — денсиметр. Но по сути это одно и то же. Ареометр состоит из наконечника, поочередно опускаемого в аккумуляторные отсеки, колбы, резиновой груши для отсасывания жидкости и шкалы измерений, которая расположена внутри колбы.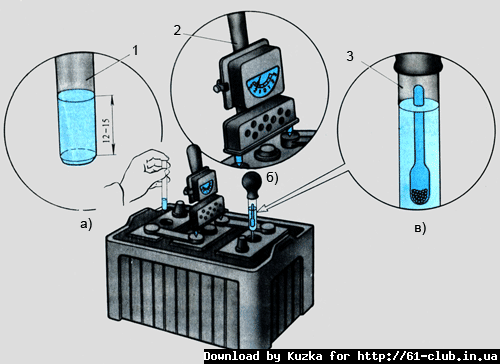
Алгоритм действий проверки будет таким:
- вытрите наконечник насухо чистой тряпочкой;
- опустите его в аккумуляторный отсек;
- резиновой грушей наберите небольшое количество жидкости;
- следите за «поведением» электролита: когда он перестанет двигаться — замерьте плотность по шкале;
- слейте жидкость обратно в «банку».
Как видите, техника снятия показаний очень проста. Главное — не забывать защитить руки с помощью перчаток.
Цифровые показатели, на которые нужно ориентироваться
Поскольку химическая составляющее АКБ напрямую зависит от температурных факторов, существуют общепринятые цифровые показатели, обозначающие уровень оптимальной концентрации электролита. На юге РФ это 1,25 , в районах средней полосы — 1,27 , а в северных регионах — 1,29 гр/см 3 .
Итак, как проверить уровень электролита в аккумуляторе и его плотность? Отнесите батарею в помещение с комнатной температурой, удалите с нее загрязнения, откройте банки и воспользуйтесь стеклянной трубочкой и ареометром. Не забудьте надеть перчатки. нужно осуществлять регулярно для обеспечения наилучшего уровня его работы.
Не забудьте надеть перчатки. нужно осуществлять регулярно для обеспечения наилучшего уровня его работы.
Ареометр — Полезные и интересные статьи об аккумуляторах в Екатеринбурге
Ареометр – это прибор, с помощью которого можно определить плотность жидкости. Работает на основании гидростатических законов, или всем нам известному закону Архимеда, согласно которому, тело, погруженное в жидкость, вытесняет ровно такой вес жидкости, которое имеет это тело. Работая с ареометром, мы без труда сможем определить содержание растворенных в жидкости веществ, в процентах. При помощи данного прибора вы сможете измерить температуру замерзания антифриза в системе охлаждения и проконтролируете плотность электролита в аккумуляторных батареях.
Ареометр представляет собой стеклянную трубку, нижняя часть которой заполняется ртутью или дробью с целью определения необходимой массы. Верхняя часть трубки проградуирована шкалой, для определения плотности раствора или концентрации растворенного вещества.
В зависимости от того, для каких жидкостей предназначены ареометры (тяжелее или легче воды), они бывают разными. Различным бывает и нанесение градуировки шкалы на прибор.
Для того чтобы предотвратить понижение уровня электролита в аккумуляторе при испарении из него воды, необходимо своевременно его проверять. Такой достаточно мудрый уход за аккумулятором, позволит вам в значительной мере увеличить срок его службы. А в выполнении этого своевременного контроля вам не обойтись без ареометра. Он в точности предоставит вам нужную своевременную информацию о плотности электролита, указывая на соотношение количества кислоты и дистиллированной воды в растворе.
Работая с ареометром необходимо осторожно опускать его в жидкость, пока вы не убедитесь, что он плавает. Перед погружением необходимо проверить температуру, ведь на ареометрах указана та температура жидкости, для какой они предназначены. Делая замеры плотности электролита в аккумуляторе при отрицательной температуре, необходимо делать поправку к показаниям, так как понижение температуры электролита на 1oC приводит к увеличению плотности на 0,0007 г/см3. Например, замерив плотность электролита при температуре -40oC можно получить результат 1,28 г/см3 – это плотность полностью заряженной батареи. Но, если привезти результат замера к температуре +25oC, мы получим результат: 1,28г/см3 — 0,0007*(40+25) = 1,23 г/см3, такая плотность соответствует 50% заряда.
Например, замерив плотность электролита при температуре -40oC можно получить результат 1,28 г/см3 – это плотность полностью заряженной батареи. Но, если привезти результат замера к температуре +25oC, мы получим результат: 1,28г/см3 — 0,0007*(40+25) = 1,23 г/см3, такая плотность соответствует 50% заряда.
Работа с ареометром начинается с того, что перед измерением его моют чистой водой, вытирают досуха полотенцем. Перед погружением в жидкость ее тщательно перемешивают. После проведения измерений прибор вторично моют, вытирают и укладывают в футляр.
Эксплуатация авто аккумулятора зимой
Что сделать, чтобы подготовить батарею к холодному времени года и какая плотность электролита нормальна для зимы?
Ответ:
У заряженной на 100% АКБ, изначально рассчитанной на использование в условиях умеренного климатического пояса, плотность электролита при стандартных +25оC должна колебаться между 1. 27 и 1.30 г/см3. Если температура будет выше, плотность снизится, если вокруг будет холоднее – повысится. Именно поэтому на крайнем Севере используют аккумуляторы с более плотным электролитом (1.32 г/см3), а в тропических странах с более низким (1.24 /см3).
27 и 1.30 г/см3. Если температура будет выше, плотность снизится, если вокруг будет холоднее – повысится. Именно поэтому на крайнем Севере используют аккумуляторы с более плотным электролитом (1.32 г/см3), а в тропических странах с более низким (1.24 /см3).
Перед наступлением холодов важно убедиться в том, что аккумулятор заряжен – в этом случае вы избежите замерзания электролита и связанных с ним проблем при пуске двигателя. Учтите также, что зимой на работу батареи серьёзное влияние оказывают утечки в системе электрооборудования и слабое натяжение генераторного ремня.
Что делать, если при старте двигателя в холода батарея разрядилась до нуля?
Ответ:
Зарядите батарею при помощи небольшого тока – причём провести зарядку нужно от стационарного устройства и не позже, чем через 2-3 дня с момента наступления глубокой разрядки.
В чём причина замерзания электролита?
Ответ:
Когда аккумулятор разряжается, плотность электролита падает – и, соответственно, становится ниже количество содержащейся в его растворе серной кислоты. Образуется вода, которая и замерзает. Чем сильнее разряжен аккумулятор, тем раньше электролит способен замёрзнуть. К примеру, при 1.11 г/см3 замерзание наступает уже при -7 градусах Цельсия, а при 1.27 г/см3 (нормальная плотность при полном заряде) только при -58 градусах.
Образуется вода, которая и замерзает. Чем сильнее разряжен аккумулятор, тем раньше электролит способен замёрзнуть. К примеру, при 1.11 г/см3 замерзание наступает уже при -7 градусах Цельсия, а при 1.27 г/см3 (нормальная плотность при полном заряде) только при -58 градусах.
Можно ли реанимировать батарею, если замёрз электролит?
Ответ:
Всё зависит от тяжести конкретного случая. Как правило, если аккумулятор замёрз не на весь объём, а его корпус не был деформирован, восстановить АКБ можно. Для этого занесите батарею в комнату, оставьте её там до тех пор, пока весь лёд не растает (это должно происходить при комнатной температуре, без лишнего нагрева), и уже после этого ставьте батарею на зарядку. Но учтите, что токовые характеристики аккумулятора в любом случае упадут, а электроды будут повреждены.
Если перед тем, как стартовать двигатель в холода, ненадолго включить фары, станет ли запуск легче?
Ответ:
Нет, это один из самых вредных мифов. Эффект разогрева электролита, на который надеются в рассматриваемом случае, будет ничтожным, а значит, мощность разряда не вырастет. Более того: батарея на этой процедуре теряет драгоценную ёмкость, и есть шанс, что оставшегося заряда на старт мотора не хватит.
Эффект разогрева электролита, на который надеются в рассматриваемом случае, будет ничтожным, а значит, мощность разряда не вырастет. Более того: батарея на этой процедуре теряет драгоценную ёмкость, и есть шанс, что оставшегося заряда на старт мотора не хватит.
Почему в холода советуют использовать аккумуляторы с высокими пусковыми токами?
Ответ:
У холодного пуска есть несколько характерных особенностей:
- 1. Стартеру понадобится больше времени на успешную прокрутку мотора;
- 2. Сопротивление холодного мотора зимой возрастает в 2.5-3 раза;
- 3. Батарее нужно будет отдать большее количество энергии и мощности;
- 4. Чем холоднее вокруг, тем выше внутреннее сопротивление АКБ.
Именно поэтому для того, чтобы двигатель стартовал надёжно, лучше использовать аккумулятор, имеющий при аналогичных габаритах более высокие токи холодной прокрутки.
На старт двигателя в холода влияет только аккумулятор?
Ответ:
Нет, влияние также оказывает состояние свечей, электрического оборудования, топливной системы и электропроводки машины. Также много зависит от качества топлива, от масла, и, конечно, от опыта водителя.
Также много зависит от качества топлива, от масла, и, конечно, от опыта водителя.
Из-за чего замёрзла батарея?
Ответ:
Если у Вас замёрзла только одна ячейка, причина, вероятно, во внутреннем дефекте аккумулятора. Из-за него в этой ячейке снизилась плотность электролита, и он замёрз.
Если замёрзло несколько ячеек, дело в том, что аккумулятор был разряжен. Чаще всего это происходит из-за того, что при поездках по городу приходится часто запускать мотор для передвижения на короткую дистанцию – генератору просто не хватает времени для того, чтобы зарядить батарею. Между тем, уже при 45% заряда аккумулятора плотность электролита будет составлять 1.21 г/см3, а при таких параметрах он замерзает уже при -30.
Часто бывает так, что утром не удаётся завести автомобиль, и водитель едет по своим делам на метро или автобусе. Тем временем, разряженная на попытках пуска батарея до вечера успеет замёрзнуть.
При зарядке аккумулятора кипит электролит – что делать?
Кипение электролита: нормально или нет?
Кипение аккумулятора можно отнести как к нормальной ситуации, так и к поводу насторожиться. Когда нормально? В случае если зарядка аккумулятора почти завершена, кипение электролита – явление нормальное. Если зарядка производится с помощью электрического тока, достаточно лишь убавить его силу, чтобы слегка уменьшить данный звук.
Когда нормально? В случае если зарядка аккумулятора почти завершена, кипение электролита – явление нормальное. Если зарядка производится с помощью электрического тока, достаточно лишь убавить его силу, чтобы слегка уменьшить данный звук.
Если электролит закипает в самом начале после соединения с зарядным устройством, это может свидетельствовать о существенных неполадках аккумулятора, которые способны привести к полному выходу устройства из строя.
Почему кипит аккумулятор
Аккумулятор – довольно простое устройство, которое, однако, имеет свои особенности. Ток в нем образуется за счет металлических (свинцовых) пластин, которые должны быть полностью погружены в электролит. Тот, в свою очередь, состоит на 35% из концентрированной серной кислоты и на оставшуюся часть – из дистиллированной воды.
При зарядке происходит химический процесс, при котором образуются пары азота и водорода. Именно образование этих пузырьков газа и их лопание создает звук, похожий на кипение. Как правило, появляется он на конечной стадии зарядки устройства, когда среда практически полностью наполнена заряженными частицами.
Как правило, появляется он на конечной стадии зарядки устройства, когда среда практически полностью наполнена заряженными частицами.
СПРАВКА. Кипение аккумулятора – это звук лопающихся пузырьков газа, которые выделяются при достаточно сильной химической активности веществ, содержащихся в электролите.
Что делать если аккумулятор кипит?
Если аккумулятор кипит при длительной зарядке от электрического тока, достаточно снизить силу тока наполовину. Кипение должно уменьшиться и можно спокойно дождаться, когда устройство зарядится полностью. Если закипать он начал в начале зарядки, это может свидетельствовать о существенных неполадках и стоит присмотреться к устройству внимательнее, немедленно отключив его от зарядного устройства.
ВНИМАНИЕ! Если аккумулятор начал сильно кипеть, нужно снизить силу тока зарядного устройства минимум наполовину.
Стандартно аккумулятор состоит из шести банок, в которых расположены свинцовые пластины. Звук кипения могут вызывать:
Звук кипения могут вызывать:
- Замкнувшие пластины;
- Расщепление пластин;
- Недостаточное количество электролита в одной или нескольких банок.
В первых двух случаях замена неисправного устройства практически неизбежна. Поэтому следует сначала отсоединить его от ЗУ, а затем отвезти либо в сервисный центр для осмотра и окончательного заключения, либо утилизировать.
В последнем случае нужно изучить качество и количество электролита. В обслуживаемых моделях посмотреть, достаточно ли жидкости, довольно просто. Достаточно открутить крышки банок и произвести визуальный осмотр. Если в одной или нескольких электролит не закрывает платины, нужно долить дистиллированной воды до нужного уровня. Доливать самостоятельно серную кислоту не рекомендуется, производить подобные операции должны только в центрах обслуживания.
Измерение плотности электролита
От плотности имеющегося в банках электролита напрямую зависит способность аккумулятора принимать заряд. Плотность замеряется только у полностью заряженного устройства, простоявшего пару часов в состоянии покоя при температуре около 25 градусов по Цельсию. Если замерять сразу после зарядки, показания окажутся завышенными.
Плотность замеряется только у полностью заряженного устройства, простоявшего пару часов в состоянии покоя при температуре около 25 градусов по Цельсию. Если замерять сразу после зарядки, показания окажутся завышенными.
Плотность измеряется в граммах на кубический сантиметр и при нормальном климате должна составлять 1,25-1,27 г/см3. В более холодных регионах ее повышают до 1,29 г/см3. Соответственно, уровень плотности в теплых регионах может быть на 0,01 ниже.
Измерить показания плотности можно самостоятельно, используя для этого специальный прибор – денсиметр. Он представляет собой стеклянную трубку, внутри которой находится ареометр. К ней присоединяется пластиковая трубка с одной стороны и резиновая груша – с другой. Для замера необходимо немного приоткрыть банку с электролитом, погрузить в нее пластиковый конец трубки и нажатием на грушу зачерпнуть немного электролита. Аэрометр покажет плотность. Подобным способом можно проверить плотность у обслуживаемой модели аккумуляторов.
Чтобы проверить данный показатель у необслуживаемого аккумулятора, который не предоставляет доступа к имеющемуся электролиту, достаточно посмотреть в специальное окошко. При нормальном уровне плотности в нем должен быть виден зеленый индикатор. При понижении плотности индикатор станет черным.
Если плотность электролита ниже нормы, это не обязательно говорит о том, что нужно его доливать. При кипении аккумулятора из жидкого состава может выпариваться только вода. Сера остается в составе, однако может скопиться вокруг свинцовых пластин, приводя к сульфатации. Если процесс еще не очень запущен и лишь небольшая часть кристаллов серы скопилась у нижнего края пластин, исправить ситуацию можно, проведя несколько циклов заряда/разряда аккумулятора.
ВАЖНО! Заливать электролит можно только в том случае, если он был пролит по неосторожности или случайности. При этом важно, чтобы плотность и температура двух составов полностью соответствовали друг другу.
Как заряжать автомобильный аккумулятор
Автомобильный аккумулятор важно уметь правильно заряжать. Для этого их различают на две категории, каждая из которых требует определенного подхода:
Для этого их различают на две категории, каждая из которых требует определенного подхода:
- Обслуживаемые аккумуляторы. В данном типе аккумуляторов нет герметизации, поэтому вода может с легкостью испаряться. Он состоит из шести банок с откручивающимися крышками, поэтому вода может из них с легкостью испаряться. Перед тем, как их заряжать необходимо произвести подготовку.
- Необслуживаемые. Батареи данного типа полностью герметичны. Испарения воды в них не происходит, так как ей просто некуда уходить. Она скапливается на стенках устройства, где конденсируется и снова опускается. Проверить уровень электролита в них можно, посмотрев на просвет. Если пластик прозрачный, можно будет оценить количество находящейся жидкой субстанции внутри.
Подготовка обслуживаемого аккумулятора
Подготовительные мероприятия включают в себя следующие действия:
- Очистку. Для этого можно использовать обычную ветошь, смоченную в растворе соды. Она удалит всю скопившуюся грязь и пыль, а также белый налет.
 Если загрязнения довольно сильные, лучше воспользоваться щеткой (неметаллической).
Если загрязнения довольно сильные, лучше воспользоваться щеткой (неметаллической). - Проверку уровня электролита. Со временем он испаряется и может неполностью покрывать пластины. Это приводит к их разрушению и дальнейшему выходу из строя всего аккумулятора. Поэтому настоятельно рекомендуется проверить и при необходимости добавить дистиллированной воды для покрытия пластин.
- Проверку плотности электролита. Она должна составлять 1,26 – 1,30 г/см3. Проверка осуществляется с помощью денсиметра. Процесс подробно описан выше.
Заряд с помощью электрического тока
Таким образом заряжают аккумуляторы, которые являются обслуживаемыми. Для этого потребуется:
- Подключить аккумулятор к зарядному устройству, соблюдая соответствие минус и плюса;
- Установить силу тока в размере 10% от емкости аккумулятора. Зарядка производится до того, как напряжение не вырастет до 14,4 В.
- Уменьшить силу тока наполовину, после чего снова оставить заряжаться до достижения напряжения 15 В.

- После этого снова снизить силу тока наполовину и заряжать аккумулятор до того, как показания силы тока и напряжения перестанут изменяться.
Способ не самый удобный и требует постоянного контроля за силой тока. Однако он позволяет добиться стопроцентного заряда аккумулятора, при этом времени на это уйдет примерно около 10-12 часов, возможно меньше. Время зарядки зависит от того, насколько сильно разрядился аккумулятор.
Заряд с помощью постоянного напряжения
Данный способ не требует постоянного контроля и внимания со стороны владельца. Здесь все регулирует сам прибор. Достаточно подсоединить аккумулятор к зарядному устройству, включить последнее, затем установить напряжение на отметке 14,5 В. И ждать. Время зарядки таким способом, как правило, составляет примерно те же 10 часов.
Не стоит держать аккумулятор на зарядке сутками, так как это способно привести к сульфатации пластин и выходу из строя устройства. Если все же нет возможности постоянно следить за уровнем заряда и регулировать силу тока, можно оставить ее на минимальном значении. Так время зарядки существенно увеличится, повреждений устройства при этом не возникнет.
Так время зарядки существенно увеличится, повреждений устройства при этом не возникнет.
Кипение аккумулятора может настораживать только в том случае, если это происходит непосредственно после подключения устройства к электрической сети. В таком случае необходимо срочно принять меры и проверить уровень содержания электролита, а также состояние пластин. После проведения профилактических мероприятий, как правило, кипение при зарядке может означать только скорое окончание этого процесса и возможность снова эксплуатировать изделие.
Уровень электролита в автомобильном аккумуляторе
От состояния аккумулятора зависит, сможете вы завести мотор своего автомобиля, или нет. Прочитав статью, вы узнаете, что влияет на уровень электролита и научитесь определять и регулировать его. Вы узнаете, как уровень электролита влияет на состояние аккумулятора и почему падение уровня снижает не только емкость, но и ресурс аккумуляторной батареи.
Что влияет на уровень электролита
Для ответа на этот вопрос, необходимо понимать, что происходит внутри аккумулятора во время заряда и разряда. При подаче зарядного тока диоксид свинца на катоде (отрицательном контакте) отдает не только свободные электроны, но и молекулы кислорода, превращаясь в свинец. На аноде (положительном электроде) наоборот, свинец впитывает из электролита электроны и молекулы кислорода, превращаясь в диоксид свинца. В обоих процессах из электролита выделяется свободный водород и незначительное количество кислорода, которые уходят в атмосферу. Чем сильней зарядный или разрядный ток, тем больше водорода и кислорода уходит в атмосферу. Помимо этого сильный зарядный или разрядный ток приводит к закипанию электролита, в результате чего в атмосферу уходит не только чистый водород и кислород, но и водяной пар. Все это со временем приводит к падению уровня электролита. Этот процесс происходит в любом аккумуляторе.
При подаче зарядного тока диоксид свинца на катоде (отрицательном контакте) отдает не только свободные электроны, но и молекулы кислорода, превращаясь в свинец. На аноде (положительном электроде) наоборот, свинец впитывает из электролита электроны и молекулы кислорода, превращаясь в диоксид свинца. В обоих процессах из электролита выделяется свободный водород и незначительное количество кислорода, которые уходят в атмосферу. Чем сильней зарядный или разрядный ток, тем больше водорода и кислорода уходит в атмосферу. Помимо этого сильный зарядный или разрядный ток приводит к закипанию электролита, в результате чего в атмосферу уходит не только чистый водород и кислород, но и водяной пар. Все это со временем приводит к падению уровня электролита. Этот процесс происходит в любом аккумуляторе.
Почему снижается уровень
Если уровень электролита падает настолько, что открывает свинцовые пластины, то ресурс аккумулятора резко снижается. Это вызвано тем, что в реакции окисления и восстановления вмешивается газообразный кислород из атмосферы. В результате баланс чистого свинца и его диоксида меняется, а вместе с ним падает емкость и рабочее напряжение аккумулятора. Добавление дистиллированной воды позволяет остановить дальнейшее разрушение пластин, но не может восстановить их состояние. Еще одна причина, по которой может падать уровень электролита – механическое повреждение корпуса. Даже небольшая трещина, которую очень сложно заметить невооруженным взглядом, может стать причиной потери электролита. При утечке в размере 1 капли в час, за месяц аккумулятор потеряет 30-50 миллилитров электролита. Примерно 0,5 литра в течение года, то есть почти весь электролит одной банки аккумулятора.
В результате баланс чистого свинца и его диоксида меняется, а вместе с ним падает емкость и рабочее напряжение аккумулятора. Добавление дистиллированной воды позволяет остановить дальнейшее разрушение пластин, но не может восстановить их состояние. Еще одна причина, по которой может падать уровень электролита – механическое повреждение корпуса. Даже небольшая трещина, которую очень сложно заметить невооруженным взглядом, может стать причиной потери электролита. При утечке в размере 1 капли в час, за месяц аккумулятор потеряет 30-50 миллилитров электролита. Примерно 0,5 литра в течение года, то есть почти весь электролит одной банки аккумулятора.
Как проверить и восстановить уровень электролита
Для проверки электролита вам понадобятся:
- чистая тряпка, чтобы очистить его поверхность от грязи;
- широкая (не менее 1 см) плоская отвертка, с помощью которой вы будете откручивать заливные пробки;
- фонарик.
Откройте капот и осмотрите аккумулятор. На некоторых автомобилях для проверки и доливки электролита приходится снимать аккумулятор. Если ничто не мешает выкручивать пробки и пользоваться фонариком, то тряпкой очистите аккумулятор от пыли, грязи и капелек жидкости. Его поверхность должна быть сухой и чистой. Если заливные пробки закрыты пластиковой накладкой, то снимите ее. Затем выкрутите все пробки и уберите их в сторону. Уровень электролита должен быть на 1,5-2 см ниже поверхности аккумулятора. Для более точной проверки уровня необходима стеклянная или пластиковая палочка. Вставьте ее в заливное отверстие и доведите до верхнего края пластин. Уровень электролита должен превышать пластины на 1,5-2 см. Если уровень ниже и, вы не видите электролит, посветите в заливное отверстие фонариком. Если видны пластины, значит, ресурс аккумулятора уже пострадал. Если восстановить уровень и плотность электролита, то он будет давать нормальный ток, но емкость снизится.
На некоторых автомобилях для проверки и доливки электролита приходится снимать аккумулятор. Если ничто не мешает выкручивать пробки и пользоваться фонариком, то тряпкой очистите аккумулятор от пыли, грязи и капелек жидкости. Его поверхность должна быть сухой и чистой. Если заливные пробки закрыты пластиковой накладкой, то снимите ее. Затем выкрутите все пробки и уберите их в сторону. Уровень электролита должен быть на 1,5-2 см ниже поверхности аккумулятора. Для более точной проверки уровня необходима стеклянная или пластиковая палочка. Вставьте ее в заливное отверстие и доведите до верхнего края пластин. Уровень электролита должен превышать пластины на 1,5-2 см. Если уровень ниже и, вы не видите электролит, посветите в заливное отверстие фонариком. Если видны пластины, значит, ресурс аккумулятора уже пострадал. Если восстановить уровень и плотность электролита, то он будет давать нормальный ток, но емкость снизится.
Если уровень электролита меньше, чем должен быть, проверьте его с помощью ареометра, который можно купить в любом автомагазине. Если плотность электролита разряженного аккумулятора ниже 1,2 г/см³, а полностью заряженного ниже 1,29 г/см³, проблема в корпусе аккумулятора. Испарение кислорода и водорода уменьшает объем, но повышает плотность электролита выше стандартной. Утечка не только снижает объем, но и не меняет плотности электролита. Аккумулятор, который теряет электролит чинить бесполезно, в большинстве случаев трещина незаметна. Иначе вокруг аккумулятора было бы мокрое пятно.
Если плотность электролита разряженного аккумулятора ниже 1,2 г/см³, а полностью заряженного ниже 1,29 г/см³, проблема в корпусе аккумулятора. Испарение кислорода и водорода уменьшает объем, но повышает плотность электролита выше стандартной. Утечка не только снижает объем, но и не меняет плотности электролита. Аккумулятор, который теряет электролит чинить бесполезно, в большинстве случаев трещина незаметна. Иначе вокруг аккумулятора было бы мокрое пятно.
Убедившись, что проблема не в утечке электролита, приступайте в восстановлению его уровня. Для этого используйте только дистиллированную воду. Желательно наливать ее с помощью лейки. Это позволит избежать разлива воды по поверхности аккумулятора и попадания в банки различных загрязняющих веществ, которые станут участниками химических реакций. Заливайте воду тонкой струйкой, это позволит избежать превышения уровня. Подняв уровень электролита, прочистите отверстие (сапун) пробки и вкрутите ее в аккумулятор. Так поступите с каждой банкой аккумулятора.
Так поступите с каждой банкой аккумулятора.
Какой тип аккумулятора установить в квадроцикл — ATV MAN
Теперь, когда у вас есть квадроцикл, вы можете начать радостный процесс обслуживания и ухода за ним. Этот процесс может показаться ошеломляющим и немного пугающим, но, если вооружить его небольшими знаниями, уход за квадроциклом может стать нормальной частью вашей повседневной жизни. Аккумулятор — один из наиболее распространенных элементов обслуживания квадроцикла. При уходе за аккумулятором квадроцикла в первую очередь следует решить, какой тип аккумулятора выбрать.К счастью, этот выбор очевиден, и, немного подумав, вы действительно можете максимально увеличить использование квадроцикла и вложения. При выборе аккумулятора для квадроцикла следует учитывать три основных типа: свинцово-кислотные (также называемые обычными), необслуживаемые аккумуляторные батареи (также называемые Absorbent Glass Mat или AGM для краткости) и литиевые батареи.
Свинцово-кислотный или обычный
Свинцово-кислотные батареи — самый распространенный тип батарей. Они существуют уже давно, поэтому их обычно называют обычными батареями.Как правило, эти батареи легко идентифицировать, потому что они представляют собой прозрачные емкости с черной крышкой, к которой прикреплены крышки. Эти батареи имеют несколько ячеек, разделенных свинцовыми пластинами, которые заряжаются аккумуляторной кислотой для питания вашего квадроцикла. Эти батареи существуют уже давно, и поэтому они также являются наиболее экономичным вариантом. Если вы думаете, что аккумуляторы для квадроциклов такие же, как автомобильные, вы сильно ошибаетесь. Обычные аккумуляторы для квадроциклов, в отличие от большинства автомобильных аккумуляторов, требуют технического обслуживания, чтобы убедиться, что они могут нормально функционировать.Основная ответственность перед вами как владельцем квадроцикла — следить за тем, чтобы уровень кислоты оставался в пределах линий заправки. Без надлежащего количества аккумуляторной кислоты между свинцовыми пластинами велика вероятность того, что квадроцикл не будет работать, потому что аккумулятор выйдет из строя.
Они существуют уже давно, поэтому их обычно называют обычными батареями.Как правило, эти батареи легко идентифицировать, потому что они представляют собой прозрачные емкости с черной крышкой, к которой прикреплены крышки. Эти батареи имеют несколько ячеек, разделенных свинцовыми пластинами, которые заряжаются аккумуляторной кислотой для питания вашего квадроцикла. Эти батареи существуют уже давно, и поэтому они также являются наиболее экономичным вариантом. Если вы думаете, что аккумуляторы для квадроциклов такие же, как автомобильные, вы сильно ошибаетесь. Обычные аккумуляторы для квадроциклов, в отличие от большинства автомобильных аккумуляторов, требуют технического обслуживания, чтобы убедиться, что они могут нормально функционировать.Основная ответственность перед вами как владельцем квадроцикла — следить за тем, чтобы уровень кислоты оставался в пределах линий заправки. Без надлежащего количества аккумуляторной кислоты между свинцовыми пластинами велика вероятность того, что квадроцикл не будет работать, потому что аккумулятор выйдет из строя. Такой объем технического обслуживания может оттолкнуть вас от выбора обычной батареи, но для этого нет никаких причин. Линии заполнения четко обозначены на контейнере, и при надлежащем уходе эти батареи могут прослужить очень долго. Поскольку внутри батареи находится рыхлая жидкость, есть вероятность, что батарея будет немного менее стабильной на каменистой местности, но в целом это обычно не замечается большинством любителей отдыха.
Такой объем технического обслуживания может оттолкнуть вас от выбора обычной батареи, но для этого нет никаких причин. Линии заполнения четко обозначены на контейнере, и при надлежащем уходе эти батареи могут прослужить очень долго. Поскольку внутри батареи находится рыхлая жидкость, есть вероятность, что батарея будет немного менее стабильной на каменистой местности, но в целом это обычно не замечается большинством любителей отдыха.
Следует отметить, что обычные аккумуляторы не готовы к установке в квадроцикл. При покупке обычного аккумулятора для квадроцикла необходимо подготовиться к тому, чтобы зарядить аккумулятор, а затем произвести его первоначальную зарядку. Это несложный процесс, но он заслуживает упоминания. Перед заправкой новой батареи важно прочитать инструкцию по эксплуатации, прилагаемую к вашей конкретной батарее, но большинство обычных батарей заполняются очень похоже. Прежде чем начать, вы можете подумать о том, чтобы заправить аккумулятор на открытом пространстве, например, на улице или в открытом гараже, потому что используемые химические вещества являются едкими и могут нанести ущерб. Если вы пролили некоторые химические вещества, вы можете нейтрализовать их с помощью пищевой соды и воды.
Если вы пролили некоторые химические вещества, вы можете нейтрализовать их с помощью пищевой соды и воды.
Несмотря на то, что каждая батарея будет поставляться с конкретными инструкциями, в целом, вот чего вы можете ожидать при заправке нового обычного аккумулятора для квадроцикла. Когда вы покупаете обычную батарею, вы заметите, что она состоит из нескольких частей. Во-первых, у вас будет батарейный отсек, который представляет собой прозрачный корпус с черным верхом и несколькими крышками сверху. Во-вторых, у вас будет контейнер, полный аккумуляторной кислоты.В-третьих, у вас будет два набора трубок: более длинная трубка, которая обычно прикрепляется к корпусу батареи постоянно и предназначена для того, чтобы помогать батарее выводить газы из батареи во время использования, а вторая, меньшая трубка представляет собой носик, который помогает заполнить кожух аккумуляторной батареи с аккумуляторной кислотой. В качестве меры безопасности во время наполнения надевайте перчатки. Когда вы будете готовы залить аккумулятор, снимите колпачки с верхней части черной крышки на корпусе аккумулятора. Есть несколько крышек, потому что они открывают доступ к различным частям батареи, которые лежат между свинцовыми пластинами батареи.Сверху емкости для кислоты аккумуляторной батареи будет два носика. Один с большим отверстием, который используют производители для заполнения емкости кислотой на заводе, и носик гораздо меньшего размера, который используется для распределения гораздо более контролируемого количества в батарею. Присоедините маленькую трубку носика к меньшей и начните заряжать аккумулятор. Обязательно заполните каждую секцию до верхней части линии заполнения, расположенной на контейнере. Лучше всего сначала заполнить все секции частично, затем постучать по боковой стороне, чтобы удалить любые вводящие в заблуждение пузырьки воздуха, а затем полностью заполнить любые секции, в которых отсутствует жидкость.Когда каждая секция батареи будет заполнена надлежащим образом, вы захотите вручную затянуть колпачки обратно на верхнюю часть корпуса батареи, и вы готовы к первоначальной зарядке батареи.
Есть несколько крышек, потому что они открывают доступ к различным частям батареи, которые лежат между свинцовыми пластинами батареи.Сверху емкости для кислоты аккумуляторной батареи будет два носика. Один с большим отверстием, который используют производители для заполнения емкости кислотой на заводе, и носик гораздо меньшего размера, который используется для распределения гораздо более контролируемого количества в батарею. Присоедините маленькую трубку носика к меньшей и начните заряжать аккумулятор. Обязательно заполните каждую секцию до верхней части линии заполнения, расположенной на контейнере. Лучше всего сначала заполнить все секции частично, затем постучать по боковой стороне, чтобы удалить любые вводящие в заблуждение пузырьки воздуха, а затем полностью заполнить любые секции, в которых отсутствует жидкость.Когда каждая секция батареи будет заполнена надлежащим образом, вы захотите вручную затянуть колпачки обратно на верхнюю часть корпуса батареи, и вы готовы к первоначальной зарядке батареи.
Во время использования ваша батарея будет заряжаться за счет использования генератора, но сначала вы должны убедиться, что устанавливаете хороший стандарт срока службы батареи. Обеспечивая надежную первую зарядку, срок службы батареи достигает 100 процентов, что позволяет ему быть наиболее эффективным при использовании на вашем квадроцикле.Зарядить аккумулятор так же просто, как кажется, но есть несколько важных моментов. Во-первых, убедитесь, что вы используете зарядное устройство, подходящее для вашей батареи. НЕ ПЫТАЙТЕСЬ ИСПОЛЬЗОВАТЬ ДЛЯ ДАННОГО ПРОЦЕССА ЗАРЯДНОЕ УСТРОЙСТВО АВТОМОБИЛЯ. Аккумуляторы для квадроциклов не такие мощные, как автомобильные, и их можно легко испортить, используя слишком мощное зарядное устройство. Вместо этого посмотрите на усилители, на которые рассчитана ваша батарея. Обычно он расположен на передней панели аккумулятора и обозначается буквами AH.Затем найдите зарядное устройство, рассчитанное на 10% ампер. Если у вас есть аккумулятор на 14 Ач, вам нужно найти зарядное устройство, рассчитанное не более чем на 1,4 Ач.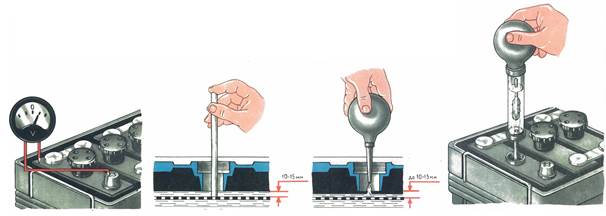 Подключите аккумулятор для зарядки, но следите за ним. Если он станет теплым на ощупь, отключите аккумулятор и дайте ему остыть, прежде чем завершить зарядку. Многие зарядные устройства имеют функции, которые автоматически отключают зарядное устройство, когда аккумулятор полностью заряжен. Если у вас нет этой функции, отключите зарядное устройство, как только зарядка будет завершена, чтобы обеспечить максимальную зарядку аккумулятора.Наконец, вы можете заметить, что уровень кислоты в вашей батарее снижается во время первоначальной зарядки в одной или нескольких секциях батареи. В этом случае осторожно открутите крышку этой секции и используйте дистиллированную воду, чтобы долить жидкость до верхней линии наполнения контейнера. Незначительное участие в первоначальной зарядке принесет дивиденды в виде продления срока службы и здоровья вашей батареи, а также инвестиций. После завершения зарядки вы готовы установить аккумулятор в квадроцикл.
Подключите аккумулятор для зарядки, но следите за ним. Если он станет теплым на ощупь, отключите аккумулятор и дайте ему остыть, прежде чем завершить зарядку. Многие зарядные устройства имеют функции, которые автоматически отключают зарядное устройство, когда аккумулятор полностью заряжен. Если у вас нет этой функции, отключите зарядное устройство, как только зарядка будет завершена, чтобы обеспечить максимальную зарядку аккумулятора.Наконец, вы можете заметить, что уровень кислоты в вашей батарее снижается во время первоначальной зарядки в одной или нескольких секциях батареи. В этом случае осторожно открутите крышку этой секции и используйте дистиллированную воду, чтобы долить жидкость до верхней линии наполнения контейнера. Незначительное участие в первоначальной зарядке принесет дивиденды в виде продления срока службы и здоровья вашей батареи, а также инвестиций. После завершения зарядки вы готовы установить аккумулятор в квадроцикл.
Необслуживаемые аккумуляторы
Второй тип аккумуляторов, который следует учитывать, называется аккумулятором, не требующим обслуживания, или аккумулятором с абсорбирующим стекломатным матом (AGM). Эти батареи называются AGM, потому что они имеют слои стекловолокна между свинцовыми пластинами, которые помогают поглощать электролиты и удерживать жидкость на месте. Это позволяет аккумулятору лучше контролировать вибрацию жидкости, что обеспечивает более стабильный выход энергии и лучшее время автономной работы, особенно для автомобилей, предназначенных для бездорожья.
Эти батареи называются AGM, потому что они имеют слои стекловолокна между свинцовыми пластинами, которые помогают поглощать электролиты и удерживать жидкость на месте. Это позволяет аккумулятору лучше контролировать вибрацию жидкости, что обеспечивает более стабильный выход энергии и лучшее время автономной работы, особенно для автомобилей, предназначенных для бездорожья.
Необслуживаемые батареи имеют ряд преимуществ по сравнению с обычными свинцово-кислотными батареями. Во-первых, они обычно меньше обычных батарей. Благодаря абсорбирующему слою между пластинами они также разряжаются с меньшей скоростью, что полезно для транспортных средств, которые с большей вероятностью будут сидеть в течение длительного периода времени. Если вы время от времени ездите на велосипеде, возможно, стоит потратить деньги, чтобы повысить вероятность того, что ваша батарея заработает после некоторого сидения.
Хотя эти батареи «не требуют обслуживания», это не обязательно означает, что они не потребуют какой-либо работы с передней частью. Многие необслуживаемые батареи поставляются заранее упакованными и готовыми к зарядке, но другим все равно потребуется, чтобы вы залили аккумулятор в корпус кислоты. Этот процесс в AGM упрощен по сравнению с обычными батареями. В упаковке вы найдете только три предмета: корпус аккумуляторной батареи, кислотный пакет и крышки для верхней части аккумуляторного блока. Батареи этих типов обычно поставляются в комплекте с кислотными батареями, поверхность которых предварительно измерена с помощью фольги. В верхней части корпуса батареи будут соответствующие точки, предназначенные для протыкания фольги, поэтому вам просто нужно перевернуть блок с кислотой, прочно проткнуть фольгу и дать кислоте стечь в батарею.После того, как батарея заполнится, есть палочка для прокола, которую вы можете использовать, чтобы проткнуть отверстие в верхней части упаковки с кислотой, чтобы позволить воздуху проникать в отсеки, что позволит жидкости стекать быстрее. Этот процесс может занять до часа, чтобы убедиться, что аккумулятор полностью заряжен.
Многие необслуживаемые батареи поставляются заранее упакованными и готовыми к зарядке, но другим все равно потребуется, чтобы вы залили аккумулятор в корпус кислоты. Этот процесс в AGM упрощен по сравнению с обычными батареями. В упаковке вы найдете только три предмета: корпус аккумуляторной батареи, кислотный пакет и крышки для верхней части аккумуляторного блока. Батареи этих типов обычно поставляются в комплекте с кислотными батареями, поверхность которых предварительно измерена с помощью фольги. В верхней части корпуса батареи будут соответствующие точки, предназначенные для протыкания фольги, поэтому вам просто нужно перевернуть блок с кислотой, прочно проткнуть фольгу и дать кислоте стечь в батарею.После того, как батарея заполнится, есть палочка для прокола, которую вы можете использовать, чтобы проткнуть отверстие в верхней части упаковки с кислотой, чтобы позволить воздуху проникать в отсеки, что позволит жидкости стекать быстрее. Этот процесс может занять до часа, чтобы убедиться, что аккумулятор полностью заряжен. Как только аккумулятор будет заполнен, закройте крышку аккумулятором сверху. Обязательно затяните эти колпачки вручную и не используйте какие-либо инструменты. После того, как аккумулятор будет заполнен, установите аккумулятор для зарядки, следуя тем же принципам, что и обычный аккумулятор.
Как только аккумулятор будет заполнен, закройте крышку аккумулятором сверху. Обязательно затяните эти колпачки вручную и не используйте какие-либо инструменты. После того, как аккумулятор будет заполнен, установите аккумулятор для зарядки, следуя тем же принципам, что и обычный аккумулятор.
Литиевые батареи
Последний тип батареи, которую следует рассмотреть для вашего квадроцикла, — это литиевая батарея. Это новейший и наиболее специализированный тип аккумулятора, который требует более существенной цены. Эти батареи поставляются запечатанными и готовы к зарядке и установке. В отличие от свинцово-кислотных и AGM-аккумуляторов, в литиевых аккумуляторах нет жидкости. Это делает их легче, меньше и их можно устанавливать в любом положении. Литиевые батареи — это новейшие разработки в области аккумуляторных батарей для квадроциклов, но это не делает их необходимыми для всех квадроциклов.Литиевая батарея — неплохое вложение, но если вы не бдительный гонщик, она может оказаться ненужной.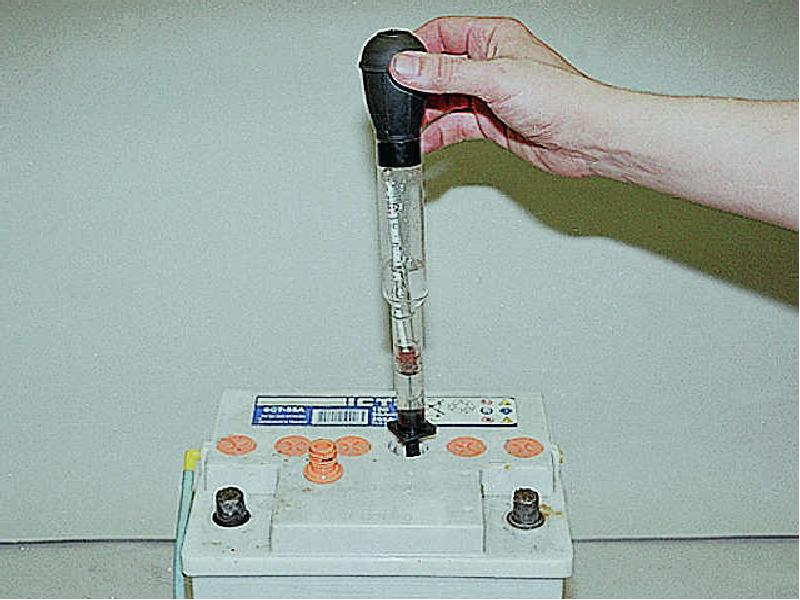
Поначалу обслуживание квадроцикла может показаться сложной задачей, и выбор типа аккумулятора не исключение. Любая батарея, которую вы выберете, станет отличным выбором для вашего квадроцикла, если вы понимаете преимущества и обязанности, связанные с каждым типом батареи. При поиске аккумулятора для вашего автомобиля уделите время рассмотрению ваших конкретных потребностей, а также ваших обязательств по техническому обслуживанию.
О компании АккумуляторыГэри Л. Бертран
Профессор химии
Университет Миссури-Ролла
Моделирование Вернуться к началу
Батарея состоит из одного или нескольких электрохимических элементов.
Каждая ячейка содержит два металлических электрода и как минимум один раствор электролита.
(раствор, содержащий ионы, которые могут проводить электричество). Батарея
действует посредством электрохимических реакций, называемых окислением и восстановлением.Эти реакции включают обмен электронами между химическими частицами. Если химическое соединение теряет один или несколько электронов, это называется окислением.
Противоположный процесс — усиление электронов — называется редукцией.
Если химическое соединение теряет один или несколько электронов, это называется окислением.
Противоположный процесс — усиление электронов — называется редукцией.
Окисление происходит на аноде.
Восстановление происходит на катоде.
Если реактивные компоненты электрохимические ячейки находятся в контакте друг с другом, они будут реагируют прямым переносом электронов ( окисление — реакция восстановления) и там невозможно использовать эту энергию для выполнения электрических работ.Большинство из энергия реакции выделяется в виде тепла. Выделяемое тепло тесно связан со стандартным изменением энтальпии (дельта-Н °) реакции.
В большинстве аккумуляторов используются разные материалы.
два электрода, так что они хотят реагировать с одним материалом,
окисляется, а другой восстанавливается. В ячейке ниже цинк
используется для электрода слева (анод), контактирующего с раствором
ионов цинка (II), возможно, раствор
Цинк
Нитрат.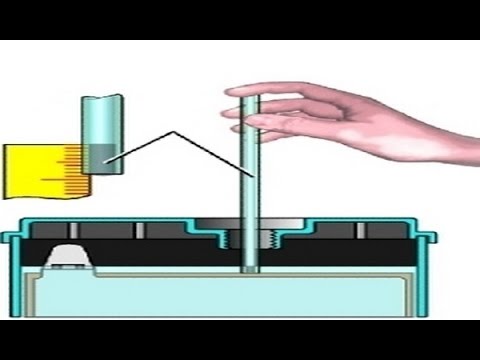 Медь используется для
электрод справа (Катод) в контакте с раствором, содержащим
Медь
(II) ионы, возможно
Нитрат меди.
Сохраняя материалы разделенными, электроны, производимые
окисление на аноде может быть использовано для выполнения электрических работ в том виде, в котором они
переносятся на катод, где они будут потребляться восстановлением
процесс. Объем электрической работы, которую может произвести аккумулятор.
тесно связано со стандартным изменением свободной энергии
(дельта-G °)
реакции.
Медь используется для
электрод справа (Катод) в контакте с раствором, содержащим
Медь
(II) ионы, возможно
Нитрат меди.
Сохраняя материалы разделенными, электроны, производимые
окисление на аноде может быть использовано для выполнения электрических работ в том виде, в котором они
переносятся на катод, где они будут потребляться восстановлением
процесс. Объем электрической работы, которую может произвести аккумулятор.
тесно связано со стандартным изменением свободной энергии
(дельта-G °)
реакции.
Однако процесс окисления дает положительный ионов или удаляет отрицательные ионы из раствора на аноде (или это может заменить один ион на более положительный), и процесс восстановления либо удаляет положительные ионы или производит отрицательные ионы в растворе на катод. В результате получаются электрически заряженные растворы, и очень быстро останавливает процесс до того, как будет перенесено измеримое количество электронов.
Ионы должны пройти путь между
два решения, чтобы электроны непрерывно текли по проводу. Это создает «ионный ток» внутри
аккумулятор с катионами (положительно — заряженный
ионы) движутся от анода к катоду, а анионы
(отрицательно заряженные ионы) движутся от катода к аноду.
Это создает «ионный ток» внутри
аккумулятор с катионами (положительно — заряженный
ионы) движутся от анода к катоду, а анионы
(отрицательно заряженные ионы) движутся от катода к аноду.
Этот путь может быть обеспечен двумя решениями контактируют друг с другом, но это позволяет диффузию всех ионов и довольно быстро «разряжает» аккумулятор.Это распространение может быть замедляется за счет разделения растворов мембраной или пористой пробкой. Все это может привести к «потенциалу жидкого перехода». из-за различной скорости движения катионов и анионов. Соль мост »может использоваться для разделения двух растворов с помощью третьего концентрированного раствор хорошо подобранных катионов и анионов, полностью устраняя «потенциал жидкого перехода». В несколько корпусах можно сконструировать батарею так, чтобы оба электрода можно было помещается в одну емкость только с одним раствором.
********************************************** *
Напряжение ячейки может зависеть от многих факторов: материалы электродов, компоненты и концентрации растворов, тип жидкостного перехода, температура и давление. В
напряжение также зависит от электрического тока, протекающего из ячейки.
Напряжение (E) и ток (I)
связаны с сопротивлением (R) через
Закон Ома: E = IR Ток напрямую связан
к скорости, с которой электроны прокачиваются через провод и любые сопротивления
в цепи.При снижении сопротивления до нуля (короткое замыкание)
ток увеличивается, а напряжение ячейки уменьшается до нуля. В качестве
сопротивление увеличивается, ток уменьшается, а напряжение увеличивается
к предельному значению. В химии,
нас в первую очередь интересует это предельное значение, максимальное напряжение
что может доставить электрохимический элемент. Этот максимум
напряжение или электрохимический
потенциал — это мера максимума
электромонтажные работы, которые можно получить от
химическая реакция, происходящая внутри клетки, и это может быть связано
к свободной энергии Гиббса
Изменения, связанные с химической реакцией.
В
напряжение также зависит от электрического тока, протекающего из ячейки.
Напряжение (E) и ток (I)
связаны с сопротивлением (R) через
Закон Ома: E = IR Ток напрямую связан
к скорости, с которой электроны прокачиваются через провод и любые сопротивления
в цепи.При снижении сопротивления до нуля (короткое замыкание)
ток увеличивается, а напряжение ячейки уменьшается до нуля. В качестве
сопротивление увеличивается, ток уменьшается, а напряжение увеличивается
к предельному значению. В химии,
нас в первую очередь интересует это предельное значение, максимальное напряжение
что может доставить электрохимический элемент. Этот максимум
напряжение или электрохимический
потенциал — это мера максимума
электромонтажные работы, которые можно получить от
химическая реакция, происходящая внутри клетки, и это может быть связано
к свободной энергии Гиббса
Изменения, связанные с химической реакцией. Прежде чем мы закончим обсуждение, обсудим термодинамику. аккумуляторов, нам необходимо учитывать влияние концентрации на напряжение
ячейки. Это может быть несколько сложным и запутанным.
Мы собираемся избежать этих проблем, сосредоточив внимание на ячейках с очень специфическим
тип химической реакции.
аккумуляторов, нам необходимо учитывать влияние концентрации на напряжение
ячейки. Это может быть несколько сложным и запутанным.
Мы собираемся избежать этих проблем, сосредоточив внимание на ячейках с очень специфическим
тип химической реакции.
********************************************** *
В ячейке выше электроны производятся свинцом. металл окисляется до ионов свинца (II), а ионы меди (II) восстанавливаются к металлической меди.Даже если ионы движутся через границу между в растворах наблюдается увеличение концентрации ионов свинца на слева и уменьшение ионов меди справа. Это вызывает напряжение батареи уменьшится, и в конечном итоге напряжение будет уменьшаются до нуля. Некоторые батареи рассчитаны на перезарядку. заставляя электроны течь назад через ячейку, обращая химическая реакция. Уравнение Нернста описывает
влияние концентраций на максимальное напряжение, которое
реакция может быть произведена путем соотнесения напряжения со стандартом
Электрохимический потенциал (E °). Этот Стандарт
Электрохимический потенциал представляет собой максимальное напряжение реакции
может производить со всеми компонентами в своем стандарте
состояния или при единичной деятельности.
Этот Стандарт
Электрохимический потенциал представляет собой максимальное напряжение реакции
может производить со всеми компонентами в своем стандарте
состояния или при единичной деятельности.
********************************************** *
Остальная часть этого обсуждения будет касаться с электрохимическими ячейками, не предполагающими изменения концентраций ионов или газов. В этих ячейках Стандарт Электрохимический потенциал можно измерить напрямую.Один из способов сделать это — использовать металл / металл. Солевые электроды, которые получают путем покрытия металла одним его нерастворимых солей (или оксида), как в Silver / Silver Хлорид, свинец / сульфат свинца или ртуть / ртуть Хлоридные (каломелевые) электроды. Эти обычно являются твердым металлом и твердой солью, хотя в случае ртути металл — чистая жидкость. Электрический контакт обычно осуществляется через платиновый провод, контактирующий с ртуть.
Эта ячейка построена с отведением / отведением
Сульфатный анод и серебро / сульфат серебра
катод, оба в растворе сульфата натрия. Два раствора разделены анионным обменом.
мембрана, которая пропускает отрицательно заряженные ионы,
но положительно заряженные ионы не могут. Напряжение этой ячейки все еще
зависит от тока, протекающего от него, и от температуры.
Однако при любой фиксированной температуре максимальное напряжение (при очень низком токе)
не зависит от концентрации электролита и равна
Стандартный электрохимический потенциал для
эта реакция.
Два раствора разделены анионным обменом.
мембрана, которая пропускает отрицательно заряженные ионы,
но положительно заряженные ионы не могут. Напряжение этой ячейки все еще
зависит от тока, протекающего от него, и от температуры.
Однако при любой фиксированной температуре максимальное напряжение (при очень низком токе)
не зависит от концентрации электролита и равна
Стандартный электрохимический потенциал для
эта реакция.
верхняя
Системы охлаждения электромобилей
В этом руководстве представлен обзор способов охлаждения литий-ионных аккумуляторных батарей и оценка того, какая система охлаждения аккумулятора является наиболее эффективной на рынке.
Обсуждает:
- Важность управления температурным режимом аккумуляторной батареи
- Четыре разные системы охлаждения:
- Материал с фазовым переходом (PCM)
- Ребристое охлаждение
- Воздушное охлаждение
- Жидкостное охлаждение (прямое и косвенное)
- Оценка того, какая система охлаждения наиболее эффективна
- Требования к жидким теплоносителям в различных системах
СКАЧАТЬ БЕСПЛАТНО
5 РАЗЛИЧИЙ МЕЖДУ ДВИГАТЕЛЯМИ EV И ДВИГАТЕЛЯМИ ВНУТРЕННЕГО СГОРАНИЯ
Система управления температурным режимом электромобиля
Важность системы охлаждения
Несмотря на то, что в аккумуляторных батареях для электромобилей были достигнуты усовершенствования, которые позволяют им обеспечивать большую мощность и требовать менее частой зарядки, одной из самых больших проблем, которые остаются для безопасности аккумуляторов, является возможность разработать эффективную систему охлаждения.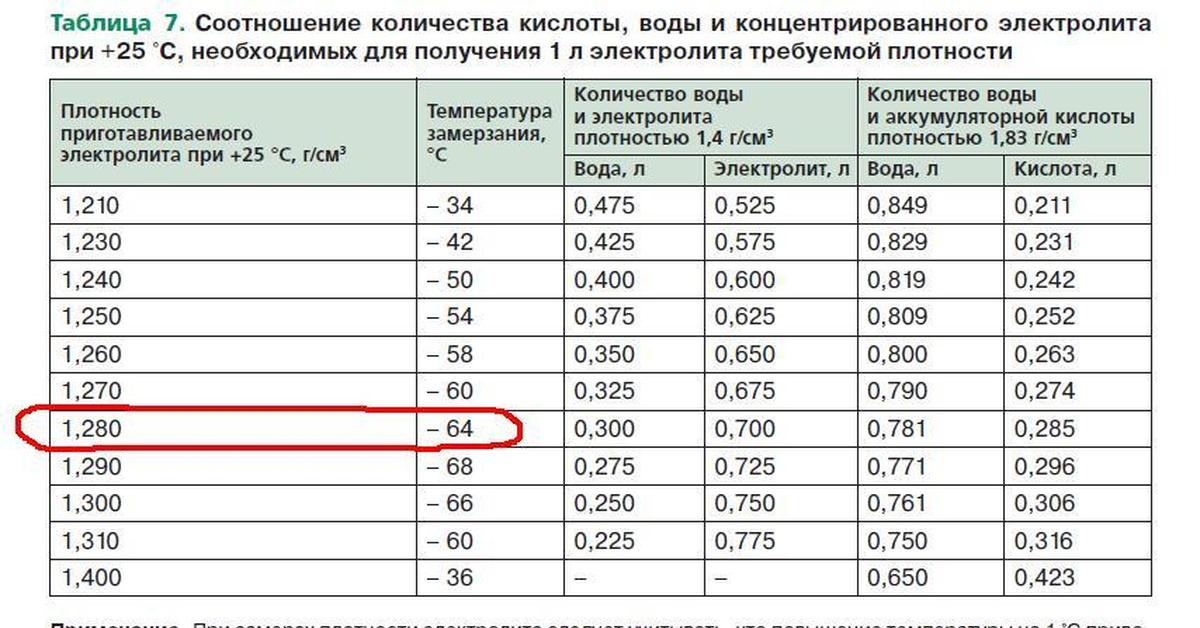
В электромобилях при разрядке аккумулятора выделяется тепло; чем быстрее вы разряжаете аккумулятор, тем больше тепла он выделяет.
Батареи работают по принципу разности напряжений, и при высоких температурах электроны внутри становятся возбужденными, что уменьшает разницу в напряжении между двумя сторонами батареи. Поскольку аккумуляторы предназначены только для работы между определенными крайними температурами, они перестанут работать, если отсутствует система охлаждения, поддерживающая их в рабочем диапазоне.Системы охлаждения должны поддерживать температуру аккумуляторной батареи в диапазоне примерно 20-40 градусов по Цельсию, а также поддерживать минимальную разницу температур внутри аккумуляторной батареи (не более 5 градусов по Цельсию).
Если существует большая внутренняя разница температур, это может привести к разной скорости заряда и разряда для каждой ячейки и ухудшить характеристики аккумуляторной батареи.
Потенциальные проблемы термической стабильности, такие как снижение емкости, тепловой разгон и пожар, могут возникнуть, если аккумулятор перегревается или если в аккумуляторном блоке наблюдается неравномерное распределение температуры. Перед лицом опасных для жизни проблем безопасности в индустрии электромобилей постоянно появляются инновации, направленные на улучшение системы охлаждения аккумуляторных батарей.
Перед лицом опасных для жизни проблем безопасности в индустрии электромобилей постоянно появляются инновации, направленные на улучшение системы охлаждения аккумуляторных батарей.
Системы охлаждения электромобилей
Какая система охлаждения лучше всего работает в электромобилях?
Системы управления температурным режимом аккумуляторных батарей все еще являются предметом тщательных исследований, и то, что мы знаем о них, будет меняться и развиваться в ближайшие годы, поскольку инженеры продолжают переосмысливать принцип работы наших автомобильных двигателей.
Есть несколько вариантов охлаждения аккумулятора электромобиля — с помощью материала с фазовым переходом, ребер, воздуха или жидкого хладагента.
Материал с фазовым переходом поглощает тепловую энергию, изменяя состояние с твердого на жидкое. При изменении фазы материал может поглощать большое количество тепла при небольшом изменении температуры.
 Системы охлаждения материала с фазовым переходом могут удовлетворить требования к охлаждению аккумуляторной батареи, однако изменение объема, которое происходит во время фазового перехода, ограничивает ее применение.Кроме того, материал с фазовым переходом может только поглощать выделяемое тепло, но не отводить его, что означает, что он не сможет снизить общую температуру, как и другие системы. Хотя материалы с фазовым переходом не подходят для использования в транспортных средствах, они могут быть полезны для улучшения тепловых характеристик в зданиях за счет уменьшения колебаний внутренней температуры и снижения пиковых охлаждающих нагрузок.
Системы охлаждения материала с фазовым переходом могут удовлетворить требования к охлаждению аккумуляторной батареи, однако изменение объема, которое происходит во время фазового перехода, ограничивает ее применение.Кроме того, материал с фазовым переходом может только поглощать выделяемое тепло, но не отводить его, что означает, что он не сможет снизить общую температуру, как и другие системы. Хотя материалы с фазовым переходом не подходят для использования в транспортных средствах, они могут быть полезны для улучшения тепловых характеристик в зданиях за счет уменьшения колебаний внутренней температуры и снижения пиковых охлаждающих нагрузок.Ребра охлаждения увеличивают площадь поверхности для увеличения скорости теплопередачи. Тепло передается от аккумуляторной батареи к ребру посредством теплопроводности и от ребра к воздуху посредством конвекции.Ребра обладают высокой теплопроводностью и могут обеспечивать охлаждение, но при этом значительно увеличивают вес упаковки.
 Использование ребер нашло большой успех в электронике, и традиционно они использовались в качестве дополнительной системы охлаждения на транспортных средствах с двигателями внутреннего сгорания. Использование ребер для охлаждения аккумулятора электромобиля вышло из употребления, поскольку дополнительный вес ребер перевешивает преимущества охлаждения.
Использование ребер нашло большой успех в электронике, и традиционно они использовались в качестве дополнительной системы охлаждения на транспортных средствах с двигателями внутреннего сгорания. Использование ребер для охлаждения аккумулятора электромобиля вышло из употребления, поскольку дополнительный вес ребер перевешивает преимущества охлаждения.Воздушное охлаждение использует принцип конвекции для отвода тепла от аккумуляторной батареи.Когда воздух проходит по поверхности, он уносит тепло, излучаемое упаковкой. Воздушное охлаждение простое и легкое, но не очень эффективное и относительно грубое по сравнению с жидкостным охлаждением. Воздушное охлаждение используется в более ранних версиях электромобилей, таких как Nissan Leaf. Поскольку электромобили в настоящее время используются все чаще, возникают проблемы безопасности с аккумуляторными блоками с чисто воздушным охлаждением, особенно в жарком климате. Другие производители автомобилей, такие как Tesla, настаивают на том, что жидкостное охлаждение — самый безопасный метод.

Жидкие охлаждающие жидкости имеют более высокую теплопроводность и теплоемкость (способность удерживать тепло в форме энергии в своих связях), чем воздух, и поэтому работают очень эффективно и обладают такими преимуществами, как компактная структура и простота размещения. Из этих вариантов жидкие охлаждающие жидкости обеспечивают наилучшую производительность для поддержания аккумуляторной батареи в правильном температурном диапазоне и однородности. Системы жидкостного охлаждения имеют свою долю проблем безопасности, связанных с утечкой и утилизацией, поскольку гликоль может быть опасен для окружающей среды при неправильном обращении.Эти системы в настоящее время используются Tesla, Jaguar и BMW, и это лишь некоторые из них.
Исследовательская группа из Национальной лаборатории возобновляемых источников энергии (США) и Национального исследовательского центра сетевых технологий активного распределения (Китай) сравнила четыре различных метода охлаждения пакетных литий-ионных ячеек: воздушное, непрямое жидкостное, прямое жидкостное и системы охлаждения ребер. . Результаты показывают, что система воздушного охлаждения требует в 2–3 раза больше энергии, чем другие методы, для поддержания той же средней температуры; система непрямого жидкостного охлаждения имеет самый низкий максимальный рост температуры; и ребристая система охлаждения добавляет около 40% дополнительного веса элемента, что имеет наибольший вес, когда четыре метода охлаждения имеют одинаковый объем.Непрямое жидкостное охлаждение является более практичной формой, чем прямое жидкостное охлаждение, хотя оно имеет несколько меньшую охлаждающую способность. ( Сравнение различных методов охлаждения для литий-ионных аккумуляторных элементов )
. Результаты показывают, что система воздушного охлаждения требует в 2–3 раза больше энергии, чем другие методы, для поддержания той же средней температуры; система непрямого жидкостного охлаждения имеет самый низкий максимальный рост температуры; и ребристая система охлаждения добавляет около 40% дополнительного веса элемента, что имеет наибольший вес, когда четыре метода охлаждения имеют одинаковый объем.Непрямое жидкостное охлаждение является более практичной формой, чем прямое жидкостное охлаждение, хотя оно имеет несколько меньшую охлаждающую способность. ( Сравнение различных методов охлаждения для литий-ионных аккумуляторных элементов )
Определяющими характеристиками системы охлаждения аккумуляторной батареи электромобиля являются температурный диапазон и однородность, энергоэффективность, размер, вес и простота использования (т. Е. Реализации, обслуживания).
Каждая из этих предлагаемых систем может быть спроектирована для достижения правильного температурного диапазона и однородности. Энергоэффективности добиться труднее, поскольку охлаждающий эффект должен быть больше, чем тепло, выделяемое при питании системы охлаждения. Кроме того, система со слишком большим дополнительным весом будет истощать энергию автомобиля, поскольку она выводит мощность.
Энергоэффективности добиться труднее, поскольку охлаждающий эффект должен быть больше, чем тепло, выделяемое при питании системы охлаждения. Кроме того, система со слишком большим дополнительным весом будет истощать энергию автомобиля, поскольку она выводит мощность.
Материал с фазовым переходом, вентиляторное охлаждение и воздушное охлаждение — все это не соответствует требованиям к энергоэффективности, размеру и весу, хотя они могут быть так же просты в реализации и обслуживании, как и жидкостное охлаждение. Жидкостное охлаждение — единственный оставшийся вариант, который не потребляет слишком много паразитной энергии, обеспечивает требования к охлаждению и компактно и легко помещается в аккумуляторную батарею.Литий-ионные аккумуляторы Tesla, BMW i-3 и i-8, Chevy Volt, Ford Focus, Jaguar i-Pace и LG Chem используют ту или иную систему жидкостного охлаждения. Поскольку электромобили все еще являются относительно новой технологией, возникали проблемы с поддержанием диапазона температур и однородности при экстремальных температурах даже при использовании системы жидкостного охлаждения.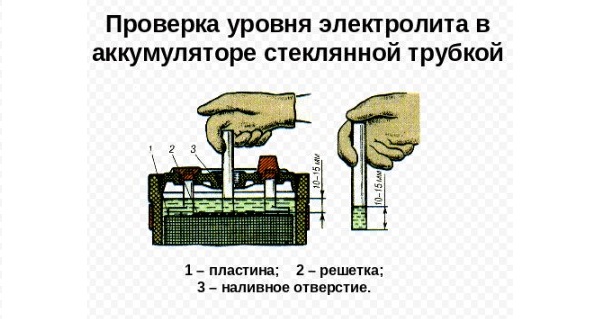 Вероятно, это связано с производственными проблемами, и по мере того, как компании приобретают опыт разработки этих систем, необходимо решать проблемы управления температурным режимом.
Вероятно, это связано с производственными проблемами, и по мере того, как компании приобретают опыт разработки этих систем, необходимо решать проблемы управления температурным режимом.
В системах жидкостного охлаждения существует другое разделение на прямое и косвенное охлаждение — независимо от того, погружены ли элементы в жидкость или если жидкость перекачивается по трубам.
В системах прямого охлаждения элементы аккумуляторной батареи находятся в непосредственном контакте с охлаждающей жидкостью. Эти схемы терморегулирования в настоящее время находятся на стадии исследований и разработок, и на рынке нет автомобилей, использующих эту систему. Непосредственного охлаждения добиться труднее из-за того, что требуется новый тип охлаждающей жидкости. Поскольку аккумулятор находится в контакте с жидкостью, охлаждающая жидкость должна иметь низкую проводимость или ее отсутствие.
Системы непрямого охлаждения похожи на системы охлаждения ДВС, в которых жидкий хладагент циркулирует по металлическим трубам.
 Однако конструкция системы охлаждения электромобилей будет выглядеть иначе. Структура системы охлаждения, которая обеспечивает максимальную однородность температуры, зависит от формы аккумуляторной батареи и будет выглядеть по-разному для каждого производителя автомобиля.
Однако конструкция системы охлаждения электромобилей будет выглядеть иначе. Структура системы охлаждения, которая обеспечивает максимальную однородность температуры, зависит от формы аккумуляторной батареи и будет выглядеть по-разному для каждого производителя автомобиля.
Требования к жидким хладагентам
Обеспечение безопасности и эффективности охлаждающих жидкостей
Учитывая, что жидкостное охлаждение является наиболее эффективным и практичным методом охлаждения аккумуляторных батарей и в настоящее время наиболее широко используемым, необходимо уделить внимание типу охлаждающей жидкости, используемой в этих системах.
Непрямое жидкостное охлаждение
Системы непрямого жидкостного охлаждения для электромобилей и обычные системы охлаждения двигателя внутреннего сгорания (ДВС) очень похожи: в обеих системах охлаждающая жидкость циркулирует по ряду металлических труб для отвода тепла от аккумуляторной батареи или двигателя. Следовательно, требования к охлаждающей жидкости для систем непрямого жидкостного охлаждения будут очень похожи на традиционные охлаждающие жидкости ДВС.
Следовательно, требования к охлаждающей жидкости для систем непрямого жидкостного охлаждения будут очень похожи на традиционные охлаждающие жидкости ДВС.
99% охлаждающей жидкости — это товар, такой как гликоль или полигликоль, но 1% -ный пакет присадок — это то, что отличает хорошую защиту двигателя от отличной защиты и производительности.При циркуляции жидкого хладагента по металлическим трубопроводам важно защитить его от коррозии для обеспечения безопасности и производительности автомобиля.
Металл очень нестабилен, поэтому он, естественно, хочет реагировать с другими элементами, теряя электроны, чтобы перейти в более стабильное состояние. Коррозия возникает из-за того, что примеси в охлаждающей жидкости имеют на себе положительный заряд, поэтому они взаимодействуют с металлическими трубами и снимают часть поверхности. Пакеты присадок можно смешивать с антифризом для образования охлаждающей жидкости, защищающей от ржавчины, накипи и коррозии.Пакеты присадок, используемые в автомобилях с ДВС, содержат ингибиторы коррозии для защиты многих типов металлов, присутствующих в системах охлаждения, таких как трубы, прокладки, соединения, радиатор и т. Д. Американское общество испытаний и материалов поддерживает стандарты, которым должны соответствовать охлаждающие жидкости для защиты от коррозия различных типов металлов. То, что в настоящее время известно о предотвращении коррозии в системах охлаждения двигателей внутреннего сгорания, можно легко применить к системе непрямого жидкостного охлаждения в электромобилях.
Д. Американское общество испытаний и материалов поддерживает стандарты, которым должны соответствовать охлаждающие жидкости для защиты от коррозия различных типов металлов. То, что в настоящее время известно о предотвращении коррозии в системах охлаждения двигателей внутреннего сгорания, можно легко применить к системе непрямого жидкостного охлаждения в электромобилях.
Прямое жидкостное охлаждение
Существуют разные требования к охлаждающей жидкости для систем прямого жидкостного охлаждения. В системах, где аккумулятор будет напрямую контактировать с охлаждающей жидкостью, например, в транспортных средствах на топливных элементах или в системах с прямым жидкостным охлаждением, охлаждающая жидкость должна быть жидкостью с низкой проводимостью или без нее. Это будет сильно отличаться от обычных охлаждающих жидкостей ДВС, которые имеют высокую проводимость. Причина, по которой требуется низкая проводимость / отсутствие проводимости, связана с безопасностью: электроны проходят через батарею, и если они подвергаются воздействию жидкости с высокой проводимостью, это приведет к отказу и взрыву. Некоторыми примерами способов поддержания низкой проводимости хладагента являются использование деионизированной воды в качестве среды для текучей среды или наличие текучей среды на несолевой основе. Эти охлаждающие жидкости с низкой проводимостью и без них находятся на ранних стадиях исследований и разработок.
Некоторыми примерами способов поддержания низкой проводимости хладагента являются использование деионизированной воды в качестве среды для текучей среды или наличие текучей среды на несолевой основе. Эти охлаждающие жидкости с низкой проводимостью и без них находятся на ранних стадиях исследований и разработок.
Будущее систем охлаждения для электромобилей
Исследования и разработки будущего охлаждения
Поскольку электромобили стали широко использоваться, существует большой спрос на более длительный срок службы батарей и более высокую выходную мощность.Чтобы достичь этого, системы терморегулирования аккумуляторной батареи должны иметь возможность отводить тепло от аккумуляторной батареи, поскольку они заряжаются и разряжаются с большей скоростью. Тепло, выделяемое при использовании аккумуляторной батареи, может представлять угрозу безопасности пассажиров. Из-за высоких нагрузок и температур, создаваемых аккумуляторами, еще более важным является наличие правильного пакета охлаждающей жидкости и присадок.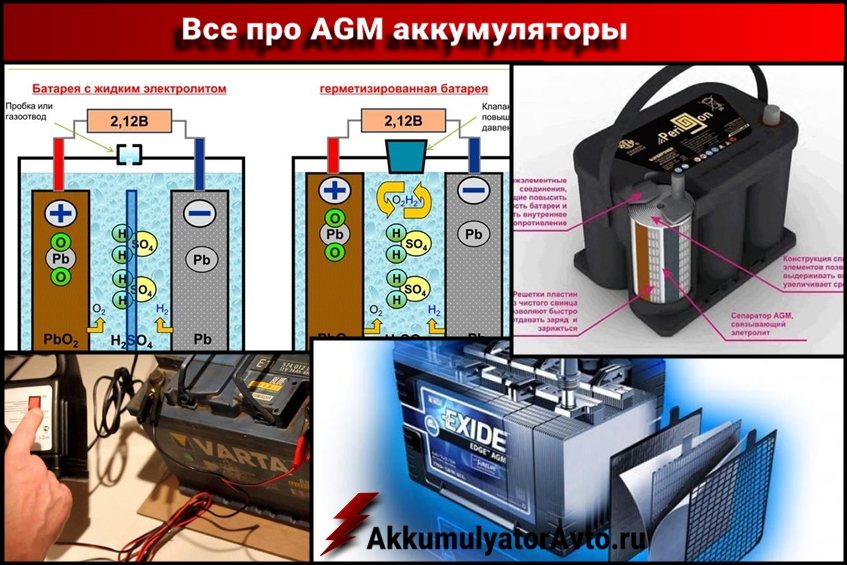 Хотя такие компании, как Tesla, BMW и LG Chem, могут использовать традиционный жидкий хладагент для своих систем непрямого охлаждения, для повышения безопасности электромобилей необходимо будет продолжать исследования и разработки в области аккумуляторных блоков и охлаждающих жидкостей.
Хотя такие компании, как Tesla, BMW и LG Chem, могут использовать традиционный жидкий хладагент для своих систем непрямого охлаждения, для повышения безопасности электромобилей необходимо будет продолжать исследования и разработки в области аккумуляторных блоков и охлаждающих жидкостей.
ВЫ ГОТОВЫ РАЗРАБОТАТЬ ЖИДКИЙ ОХЛАЖДАЮЩИЙ ЖИДКОСТЬ?
Если вы заинтересованы в разработке жидкой охлаждающей жидкости, обратитесь к ведущему поставщику антикоррозионных присадок, например, Dober.
Новые жидкометаллические батареи, работающие при комнатной температуре, могут стать источником энергии в будущем — ScienceDaily
Исследователи из инженерной школы Кокрелла Техасского университета в Остине создали новый тип батареи, сочетающий в себе многие преимущества существующих варианты при устранении их основных недостатков и экономии энергии.
Большинство батарей состоит либо из твердотельных электродов, таких как литий-ионные батареи для портативной электроники, либо из жидких электродов, включая проточные батареи для интеллектуальных сетей. Исследователи UT создали то, что они называют «полностью жидкометаллическими батареями при комнатной температуре», которые включают в себя лучшее из обоих миров жидких и твердотельных батарей.
Твердотельные батареи обладают значительной емкостью для хранения энергии, но они обычно сталкиваются с многочисленными проблемами, которые со временем приводят к их разложению и снижению эффективности.Жидкостные батареи могут доставлять энергию более эффективно, без длительного разрушения устройств в готовом состоянии, но они либо не соответствуют высоким требованиям к энергии, либо требуют значительных ресурсов для постоянного нагрева электродов и поддержания их в расплавленном состоянии.
Металлические электроды в батарее группы могут оставаться в жидком состоянии при температуре 20 градусов по Цельсию (68 градусов по Фаренгейту), что является самой низкой рабочей температурой, когда-либо зарегистрированной для жидкометаллической батареи, по словам исследователей. Это представляет собой серьезное изменение, потому что современные жидкометаллические батареи должны храниться при температуре выше 240 градусов Цельсия.
«Эта батарея может обеспечить все преимущества как твердого, так и жидкого состояния, включая больше энергии, повышенную стабильность и гибкость — без соответствующих недостатков, а также экономит энергию», — сказал Юй Дин, доктор наук, доцент. Исследовательская группа Гуйхуа Ю на факультете машиностроения Уолкера. Дин является ведущим автором статьи о батареях при комнатной температуре, недавно опубликованной командой в Advanced Materials .
Батарея включает сплав натрия и калия в качестве анода и сплав на основе галлия в качестве катода.В статье исследователи отмечают, что возможно создать батарею с еще более низкими температурами плавления, используя другие материалы.
Батарея, работающая при комнатной температуре, обещает больше энергии, чем современные литий-ионные батареи, которые составляют основу большей части персональной электроники. По словам исследователей, он может заряжать и доставлять энергию в несколько раз быстрее.
Из-за жидких компонентов аккумулятор можно легко увеличить или уменьшить в зависимости от необходимой мощности. Чем больше аккумулятор, тем большую мощность он может выдать.Такая гибкость позволяет этим батареям потенциально питать все, от смартфонов и часов до инфраструктуры, лежащей в основе движения к возобновляемым источникам энергии.
«Мы рады видеть, что жидкий металл может стать многообещающей альтернативой замене обычных электродов», — сказал профессор Ю. «Учитывая продемонстрированные высокие показатели энергии и удельной мощности, этот инновационный элемент может быть потенциально использован как для интеллектуальной сети, так и для носимой электроники».
Исследователи потратили на этот проект более трех лет, но работа еще не завершена.Многие элементы, составляющие основу этой новой батареи, более многочисленны, чем некоторые из ключевых материалов в традиционных батареях, что делает их потенциально более легкими и менее дорогостоящими в производстве в больших масштабах. Однако галлий остается дорогим материалом. Поиск альтернативных материалов, которые могут обеспечить такие же характеристики при снижении стоимости производства, остается ключевой задачей.
Следующим шагом к увеличению мощности батареи при комнатной температуре является улучшение электролитов — компонентов, которые позволяют электрическому заряду проходить через батарею.
«Хотя наша батарея не может конкурировать с высокотемпературными жидкометаллическими батареями на данном этапе, ожидается, что лучшая мощность будет, если усовершенствованные электролиты будут разработаны с высокой проводимостью», — сказал Дин.
История Источник:
Материалы предоставлены Техасским университетом в Остине . Примечание. Содержимое можно редактировать по стилю и длине.
Проблемы с аккумулятором для электронных сигарет
Батарея разряжена и не загорается
Большинство стандартных аккумуляторов электронных сигарет включаются и выключаются с помощью функции 5 щелчков (5 быстрых щелчков в течение 2 секунд).Это означает, что щелчки довольно быстрые и должны быть очень осознанными, и это часть их дизайна, чтобы они не включались без вашего ведома.
Самый простой способ сделать это — сосчитать один, два, три и т. Д. И убедиться, что вы щелкнули 5 раз, иначе батарея может не понять, что вы щелкнули 5 раз.
Батарея сообщит вам о том, что вы ее включили, мигнув 3 раза (это может быть разным, а количество миганий будет зависеть от батареи).
Батареи рассчитаны примерно на 300 перезарядок
Средняя батарея для электронных сигарет имеет типичный срок службы 300 зарядов, и этот срок службы значительно сокращается, если батареи часто заряжаются и используются постоянно.
Эти литий-ионные аккумуляторы для электронных сигарет также очень чувствительны к условиям окружающей среды из-за микротехнологии внутри них. Возможные причины разряда батареи включают проблемы с контактами, неисправную батарею, чрезмерное использование, неправильное использование, повреждение, условия окружающей среды и превышение срока службы.
Если вы все еще застряли, следующие варианты могут помочь, однако, в зависимости от вашей проблемы, часто лучше просто купить новую батарею на всякий случай.
1. Поместите аккумулятор в комнату с постоянной температурой на 24 часа (не замораживайте и не перегревайте).
2. Попробуйте зарядить аккумулятор (убедитесь, что ваше зарядное устройство работает от других совместимых аккумуляторов, иначе ваше зарядное устройство может быть проблемой).
3. Если аккумулятор заряжается, попробуйте установить другой резервуар.Если у вас все еще есть та же проблема, вполне вероятно, что причиной вашей проблемы является аккумулятор, но вы не будете точно знать, в чем проблема с аккумулятором на данном этапе.
4. Когда батарея подходит к концу, вы все равно сможете ее зарядить, но она не обязательно сможет что-либо нагреть в достаточной степени.
5. Если аккумулятор неисправен, использовался чрезмерно, неправильно, поврежден или срок его службы превысил, его не следует использовать повторно, однако, если у вас нет причин подозревать любую из этих проблем, проблема может заключаться в плохом соединении между контакт батареи и точки контакта резервуара, так как продукты могут незначительно отличаться, а также иногда точки могут слишком сильно вдавиться при свинчивании.
6. Возьмите что-нибудь вроде деревянной палочки для коктейля или кусочка кредитной карты (не используйте металлические предметы на батарее) и аккуратно приподнимите центральный контакт как на баке, так и на батарее, насколько это возможно. Это кропотливая работа, поэтому будьте осторожны, чтобы ничего не вышло не на своем месте. Для баков стиля 510 с выступающим винтом немного открутите его.
E-жидкость в аккумуляторе
Если вы попадете в аккумуляторную батарею, она может застрять во включенном или выключенном положении, что сделает ее непригодной для использования.Светодиодная кнопка часто все еще нажимается, но жидкость все еще может вывести ее из строя. Однако вы можете обнаружить, что он снова начинает работать через несколько дней, когда ему дают высохнуть. Попробуйте аккуратно постучать аккумулятором по бумажному полотенцу, если вокруг кнопки скопилась жидкость. Не нажимайте кнопку напрямую, особенно на твердой поверхности, иначе вы можете ее повредить.
Хороший чистый контакт между батареей электронной сигареты и резервуаром необходим для наилучшего нагрева, пара и аромата, поэтому необходима регулярная чистка (например, каждые пару недель).Спирт / хирургический спирт на ватной палочке / ватной палочке идеален.
Очистите внешнюю часть области соединения / контакта, а также внутреннюю часть, убедившись, что вы держите аккумулятор вверх ногами, чтобы сила тяжести могла удалить излишки жидкости. При необходимости вы можете высушить пораженное место бумажным полотенцем.
Для стойких загрязнений идеально подходит коктейльная палочка для резьбовых канавок, стараясь не сломать ее внутри аккумулятора. НЕ используйте ничего из металла.
Аккумулятор остается включенным (светодиод постоянно светится)
Существует несколько возможных причин, включая повреждение аккумулятора и заедание реле давления аккумулятора, что может привести к заклиниванию микрочипа.Если вы не можете вытащить его, вам понадобится новая батарея.
1. Несколько раз постучите концом батареи со светодиодным индикатором о твердую плоскую поверхность (не слишком сильно, только достаточно сильно, чтобы дать ей встряхнуть) и посмотрите, не погас ли светодиод. В случае неудачи перейдите к
2. Снимите бак с аккумуляторной батареи. Подуйте прямо в батарею и вдохните от нее, но выдохните этот воздух; не глотай этот воздух. Повторите это 3-4 раза или больше. В случае неудачи перейдите к
3. Подуйте и вдохните светящийся светодиодный наконечник.При необходимости повторите это как минимум 3-4 раза. В случае неудачи перейдите по номеру
4. Это последнее средство. Дайте аккумулятору полностью разрядиться, что может занять несколько часов. Когда светодиод перестанет светиться, зарядите его как обычно. При отключении питания аккумулятор может самостоятельно высвободиться. Этот шаг является крайней мерой, так как литий-ионные батареи не должны полностью разряжаться. Если этот последний шаг также не увенчался успехом, возможно, вам понадобится новый аккумулятор.
5. Примечание. Не оставляйте батареи заряженными на ночь.После полной зарядки выньте аккумулятор из зарядного устройства и отключите питание зарядного устройства.
6. Также убедитесь, что вы не храните аккумуляторы в карманах или других местах с большим количеством пыли. Пыль, обычно находящаяся в карманах, попадет внутрь аккумулятора и может вызвать неисправность переключателя.
Батарея не держит заряд
Батареи имеют ограниченный срок службы, поэтому они не будут работать вечно. Срок их службы варьируется, в среднем около 300 циклов заряда / разряда.Однако, если батарея относительно новая и не держит заряд, скорее всего, она неисправна или повреждена.
Аккумулятор заряжается нормально, светодиод светится при нажатии, но нет пара.
Скорее всего, это связано с точками контакта между аккумулятором и распылителем или это может быть головка распылителя / головка катушки. См. Нашу страницу об устранении неполадок, связанных с отсутствием или потерей паров (щелкните здесь).
Светодиодный индикатор батареи горит, но мигает при рисовании
Точка отключения батареи для электронных сигарет может быть от 5 до 10 секунд в зависимости от элемента.Это стандартная функция безопасности, поскольку батареи предназначены для отключения во избежание перегрева.
Светодиод батареи мигает 3 раза
Некоторые батареи мигают 3 раза, указывая на короткое замыкание. Большинство стандартных аккумуляторов для электронных сигарет имеют так называемую защиту от короткого замыкания, поэтому, когда происходит короткое замыкание, и вы нажимаете кнопку огня, она просто мигает 3 раза, а затем ничего не делает.
Он все еще мигает 3 раза без бака? (снимите бак, убедитесь, что батарея включена, и нажмите кнопку огня, чтобы проверить).
Если светодиод по-прежнему мигает 3 раза без резервуара, вы знаете, что это связано с аккумулятором, если он мигает только при подключении к резервуару, это может быть из-за плохого соединения, или это может быть головка катушки.
Если бак закручивается слишком сильно, центральный штифт аккумулятора может чуть чуть опустить вниз, и соединение будет потеряно. Просто убедитесь, что аккумулятор не прикручен слишком сильно. Попробуйте немного отступить и посмотрите, что произойдет.
Также попробуйте другую катушку на случай, если возникнет проблема, в зависимости от того, что вы уже обнаружили выше.
Батарея быстро мигает, но не испаряется.
Батарея разряжена и требует подзарядки. Большинство стандартных батареек для электронных сигарет мигают, как правило, быстро, чтобы вы знали, что у них заканчивается заряд.
Батарея мигает (синий?) При нажатии кнопки огня, но ничего не происходит
Aspire K3, например, будет мигать синим цветом при нажатии кнопки включения, но ничего не произойдет, когда он обнаружит неправильную катушку. Если вы используете Aspire Nautilus 0.7 с батареей K3, она не будет работать, потому что сопротивление слишком низкое для безопасного использования батареи.
Батарея активируется сама по себе
Это обычное дело для автоматических батарей (которые становятся все более редкими). Одно из решений — взять конец золы и буквально нанести им пару хороших жестких ударов по твердой поверхности.
Это может помочь вернуть механизм переключателя в правильное положение, но не всегда работает.
Не кладите скрепки или другие предметы внутрь батареи и не используйте сжатый воздух.Это может привести к необратимому повреждению переключателя. Также убедитесь, что вы не храните батарейки в карманах или других местах с большим количеством пыли.
Пыль из карманов попадет внутрь аккумулятора и может вызвать неисправность переключателя. Аккумулятор также может иногда попадать внутрь небольшого количества жидкости, что приводит к его неисправности.
Батареи часто работают нормально, если вы даете им время высохнуть, поэтому положите батарею в безопасное место и просто дайте ей постоять в течение дня или двух.
Аккумулятор сильно нагревается при использовании или зарядке
Это признак серьезной проблемы аккумулятора. НЕ ВЫБРАСЫВАЙТЕ ЕГО В УЗОР! Поместите аккумулятор в место для охлаждения, где он не представляет опасности возгорания, и не пытайтесь использовать этот аккумулятор снова.
Аккумулятор горит зеленым светом во время зарядки
Зеленый цвет означает, что аккумулятор заряжен, поэтому заряжать его больше не нужно. Все батареи поставляются частично заряженными, и вы сможете сразу же использовать их без необходимости немедленной зарядки.
Светодиодный индикатор аккумулятора мигает зеленым и красным
Аккумулятор почти полностью заряжен. Он просто сообщает, что он почти заряжен.
Батарея / мод считывает «распылитель коротко» «нет распылителя» «проверьте распылитель»
Это сообщение информирует вас о том, что существует проблема с соединением между вашей батареей (мод), мод — это аккумулятор от Кстати, и бак или катушка (форсунка).
Прежде чем мы рассмотрим решения, убедитесь, что сопротивление катушки находится в пределах возможностей вашего аккумулятора / мода.Если, допустим, катушка имеет сопротивление 0,15 Ом, а ваш мод аккумулятор может работать только до 0,5 Ом, он не будет и не должен работать по важным причинам безопасности. Если у вас есть мод, на вашем светодиодном дисплее появится сообщение. Если у вас стандартная трубчатая батарея, обычно нет дисплея, поэтому вы не увидите сообщения.
Не используйте катушки с низким сопротивлением, особенно не ниже 1,0 Ом, на стандартных трубчатых батареях. Использование катушек с низким сопротивлением в этих батареях может вызвать перегрев и привести к взрыву.
Предполагая, что у вас есть соответствующее сопротивление катушки для вашего аккумулятора / мода, вот несколько вещей, которые вы можете попробовать, чтобы решить вашу проблему:
Снимите катушку с бака и переустановите ее, иногда все просто снова начинает работать.
Очистите основание вашего резервуара (и катушку, если она выступает через основание резервуара, некоторые делают, а большинство нет), а также очистите и высушите область подключения вашей батареи. Для этого подойдет кухонное полотенце, но не туалетный рулон! Если после полной и тщательной очистки у вас остались такие же показания, попробуйте новую катушку, так как это может быть проблема с катушкой.
Иногда контакт на батарее / модуле может надавить и остаться в нижнем положении и, следовательно, не сможет установить необходимое соединение. Мы рассмотрели эту тему выше.
Для тех, кто использует перестраиваемые распылители, убедитесь, что катушка не соприкасается с какими-либо металлическими частями, которых не должно быть, а также убедитесь, что катушка не повреждена. Убедитесь, что винты стойки также правильно затянуты.
Для некоторых катушек, в частности катушек субомного сопротивления, вы можете попробовать немного отрегулировать основание катушки, а затем снова собрать резервуар вместе с катушкой на месте, просто чтобы посмотреть, позволяет ли это выполнить соединение. .Не пытайтесь раздвинуть катушку с силой, если кажется, что она не разбирается относительно легко, но у многих катушек есть основание, которое просто надвигается во время производственного процесса.
Плохие катушки встречаются нечасто, но они существуют. При необходимости попробуйте использовать другой из вашего пакета, но оставьте оригинал на всякий случай, если вам нужно вернуться к нему.
Вы также можете попробовать использовать другой резервуар, чтобы устранить причину, например, если вы знаете, что у вас есть резервуар, работающий нормально на другом аккумуляторе / моде, и он не будет работать на рассматриваемом устройстве, то он указывает на аккумулятор. / мод, о котором идет речь, является причиной проблемы.
Если вы считаете, что аккумулятор / мод неисправен, проверьте свою гарантию, которая обычно составляет 90 дней, и свяжитесь со своим поставщиком, если ваша гарантия еще действительна.
Зарядное устройство — светодиодный индикатор зарядного устройства USB мигает синим и красным цветом
Аккумулятор почти полностью заряжен. Он просто сообщает вам, что он почти заряжен (светодиод на некоторых зарядных устройствах USB становится синим, когда зарядка завершена).
Нужна новая батарея? Щелкните здесь (внутренняя ссылка на нашем сайте).
Важные примечания о зарядке аккумуляторов
— Всегда используйте правильное зарядное устройство для аккумулятора, который вы заряжаете.Никогда не оставляйте батареи без присмотра во время зарядки, отключайте их от сети перед сном или выходом на улицу.
— Не заряжайте аккумуляторы на горючих поверхностях, таких как ковры, или на поверхностях, которые могут быть повреждены теплом.
— Когда аккумулятор полностью заряжен, отключите его. В идеале после зарядки дайте аккумулятору отдохнуть в течение нескольких часов.
— Не позволяйте батарее полностью разряжаться, рекомендуется заряжать батарею, когда она разряжена, а не полностью разряжена.
— Не оставляйте аккумулятор без питания, когда он не используется — это может привести к тому, что аккумулятор станет менее пригодным для использования.
— Не нагревайте и не сжигайте батареи.
— Не заряжайте поврежденные батареи.
— Если аккумулятор нагревается во время зарядки, немедленно прекратите зарядку и дайте ему остыть, прежде чем обращаться с ним дальше.
Как хранить аккумуляторы и ухаживать за ними
Правильное хранение аккумуляторов продлевает срок их службы и предохраняет их от опасности.
— Храните батареи вдали от металлических предметов, включая такие предметы, как ключи и монеты (так что не оставляйте их в кармане).
— Храните батареи в сухом прохладном месте, не подверженном резким перепадам температуры или влажности. Если вы живете в жарком месте, батареи можно хранить в холодильнике (но не замораживайте их). Если вы сделаете это, вы должны запечатать их в герметичном пластиковом пакете, чтобы поддерживать необходимый уровень влажности.
— При хранении литиевых батарей в течение определенного периода времени, в идеале оставляйте их заряженными примерно на 40% — это минимизирует деградацию и позволяет батарее медленно разряжаться, что имеет решающее значение для ее работоспособности.
— Всегда храните батареи так, чтобы положительный и отрицательный полюсы находились подальше друг от друга, чтобы они не начали проводить электричество вхолостую.
— Не храните новые и старые батареи вместе, потому что есть риск того, что новые батареи будут проводить электричество в старые.
— Утилизируйте батареи безопасно и в соответствии с правилами (в некоторых местных магазинах сейчас есть предприятия по переработке).
Синтез, характеристика и применение негорючей дикатионной ионной жидкости в литий-ионной батарее в качестве добавки к электролиту
Сюй, К. Неводные жидкие электролиты для литиевых аккумуляторных батарей. Chemical Reviews 104 , 4303–4418, https://doi.org/10.1021/cr030203g (2004).
CAS Статья PubMed Google ученый
Armand, M. & Tarascon, J.-M. Строим батареи лучше. природа 451 , 652 (2008).
ADS CAS PubMed Статья Google ученый
Park, J.-K. Принципы и применение литиевых вторичных батарей . (John Wiley & Sons, 2012).
Glaize, C. & Genies, S. Литиевые батареи и другие электрохимические системы хранения . (John Wiley & Sons, 2013).
Guerfi, A. et al. . Улучшенные электролиты для литий-ионных аккумуляторов: смесь ионной жидкости и органического электролита с повышенной безопасностью и электрохимическими характеристиками. Журнал источников энергии 195 , 845–852 (2010).
ADS CAS Статья Google ученый
Люкс, С. и др. . Механизм образования HF в органических карбонатных электролитах на основе LiPF6. Electrochemistry Communications 14 , 47–50 (2012).
CAS Статья Google ученый
Вагнер, Р., Прещичек, Н., Пассерини, С., Лекер, Дж. И Винтер, М.Современные тенденции и перспективы исследований различных материалов и конструкций, используемых в литиевых батареях. Журнал прикладной электрохимии 43 , 481–496 (2013).
CAS Статья Google ученый
Schmitz, R. W. et al. . Исследования новых электролитов, растворителей и добавок SEI для использования в литий-ионных батареях: систематическая электрохимическая характеристика и подробный анализ спектроскопическими методами. Успехи химии твердого тела 42 , 65–84 (2014).
CAS Статья Google ученый
Скросати Б., Абрахам К., ван Шалквейк В. А. и Хассун Дж. Литиевые батареи: передовые технологии и приложения . Vol. 58 (John Wiley & Sons, 2013).
Zhang, S. S. Обзор электролитных добавок для литий-ионных аккумуляторов. Журнал источников энергии 162 , 1379–1394 (2006).
ADS CAS Статья Google ученый
Арбицани К., Габриэлли Г. и Мастрагостино М. Термическая стабильность и воспламеняемость электролитов для литий-ионных аккумуляторов. Журнал источников энергии 196 , 4801–4805 (2011).
ADS CAS Статья Google ученый
Хан, Й.-К., Ю, Дж. И Йим, Т. Почему трис (триметилсилил) фосфит эффективен в качестве добавки для высоковольтных литий-ионных батарей? Журнал химии материалов A 3 , 10900–10909 (2015).
CAS Статья Google ученый
Канг К. С. и др. . Влияние добавок на электрохимические характеристики оксида лития, никеля, кобальта, марганца при высоких температурах. Журнал источников энергии 253 , 48–54 (2014).
ADS CAS Статья Google ученый
Srour, H. et al. . Ионные жидкие электролиты для литий-ионных аккумуляторов: обзор характеристик различных электродных систем. Журнал прикладной электрохимии 46 , 149–155 (2016).
CAS Статья Google ученый
Haregewoin, A. M., Wotango, A. S. & Hwang, B.-J. Электролитические добавки для электродов литий-ионных аккумуляторов: успехи и перспективы. Энергетика и экология 9 , 1955–1988 (2016).
CAS Статья Google ученый
Балакришнан П., Рамеш Р. и Кумар Т. П. Защитные механизмы в литий-ионных батареях. Журнал источников энергии 155 , 401–414 (2006).
ADS CAS Статья Google ученый
Даути, Д. Х. и Рот, Э. П. Общее обсуждение безопасности литий-ионных аккумуляторов. Интерфейс электрохимического общества 21 , 37–44 (2012).
CAS Google ученый
Рот, Э. П. и Орендорф, К. Дж. Как электролиты влияют на безопасность аккумуляторной батареи. Интерфейс электрохимического общества 21 , 45–49 (2012).
CAS Статья Google ученый
Калхофф Дж., Эшету Г. Г., Брессер Д. и Пассерини С. Более безопасные электролиты для литий-ионных батарей: современное состояние и перспективы. ChemSusChem 8 , 2154–2175 (2015).
CAS PubMed Статья Google ученый
Чжан, Х. и др. . Последние достижения в области передовых электродных материалов, сепараторов и электролитов для литиевых батарей. Журнал химии материалов A 6 , 20564–20620 (2018).
CAS Статья Google ученый
Chen, S., Wen, K., Fan, J., Bando, Y. & Golberg, D. Прогресс и перспективы использования высоковольтных и высокобезопасных электролитов в современных литиевых батареях: из жидкости к твердым электролитам. Журнал химии материалов A 6 , 11631–11663 (2018).
CAS Статья Google ученый
Ye, Y.-S., Rick, J. & Hwang, B.-J. Ионные жидкие полимерные электролиты. Журнал химии материалов A 1 , 2719–2743 (2013).
CAS Статья Google ученый
Kim, H.-T. и др. .Ионная жидкость на основе пирролиния как антипирен для бинарных электролитов литий-ионных аккумуляторов. ACS Sustainable Chemistry & Engineering 4 , 497–505 (2015).
Артикул CAS Google ученый
Mun, J. et al. . Возможность использования ионного жидкого растворителя на основе пирролидиния для неграфитовых углеродных электродов. Электрохимические коммуникации 13 , 1256–1259 (2011).
CAS Статья Google ученый
Д’Анджело, А. Дж. И Панцер, М. Дж. Разработка эластичных и самовосстанавливающихся гелевых электролитов с использованием полностью цвиттерионных полимерных сетей в сольватно-ионных жидкостях для литиевых батарей. Химия материалов 31 , 2913–2922 (2019).
Артикул CAS Google ученый
Kim, G.-T. и др. . Разработка прототипов литиевых батарей на основе ионной жидкости. Журнал источников энергии 199 , 239–246 (2012).
CAS Статья Google ученый
Garcia, B., Lavallée, S., Perron, G., Michot, C. & Armand, M. Расплавленные соли при комнатной температуре в качестве электролита литиевых батарей. Electrochimica Acta 49 , 4583–4588 (2004).
CAS Статья Google ученый
Сакаэбе, Х. и Мацумото, Х. N-Метил-N-пропилпиперидин бис (трифторметансульфонил) имид (PP13 – TFSI) — новая электролитная основа для литиевой батареи. Electrochemistry Communications 5 , 594–598 (2003).
CAS Статья Google ученый
Де Соуза, Р. Ф., Падилья, Дж. К., Гонсалвес, Р. С. и Дюпон, Дж. Топливные элементы на основе диалкилимидазолиевой ионной жидкости при комнатной температуре. Electrochemistry Communications 5 , 728–731 (2003).
Артикул CAS Google ученый
Kunze, M. et al . Смеси ионных жидкостей для низкотемпературных электролитов. Electrochimica Acta 82 , 69–74 (2012).
CAS Статья Google ученый
Куриг, Х., Вестли, М., Тонурист, К., Янес, А. и Люст, Э. Влияние химического состава ионно-жидких анионов при комнатной температуре и делокализации электрического заряда на свойства суперконденсатора. Журнал Электрохимического общества 159 , A944 – A951 (2012).
CAS Статья Google ученый
Lei, Z. et al. . Суперконденсатор с высокой плотностью энергии с графеном – CMK-5 в качестве электрода и ионной жидкостью в качестве электролита. Журнал химии материалов A 1 , 2313–2321 (2013).
CAS Статья Google ученый
Велтон Т. Ионные жидкости при комнатной температуре. Растворители для синтеза и катализа. Химические обзоры 99 , 2071–2084 (1999).
CAS PubMed Статья Google ученый
Дюпон, Дж., Де Соуза, Р. Ф. и Суарес, П. А. Металлоорганический катализ в ионной жидкой (расплавленной соли) фазе. Химические обзоры 102 , 3667–3692 (2002).
CAS PubMed Статья Google ученый
Йим, Т., Квон, М. С., Мун, Дж. И Ли, К. Т. Электролиты на основе ионной жидкости при комнатной температуре как альтернатива электролитам на основе карбонатов. Израильский химический журнал 55 , 586–598 (2015).
CAS Статья Google ученый
Соави, Ф., Монако, С. и Мастрагостино, М. Катод из пористого углерода и ионная жидкость без катализаторов для высокоэффективных перезаряжаемых литий-кислородных батарей. Журнал источников энергии 224 , 115–119 (2013).
CAS Статья Google ученый
Бест А., Бхатт А. и Холленкамп А. Ионные жидкости с анионом бис (фторсульфонил) имида: электрохимические свойства и применение в аккумуляторной технологии. Журнал Электрохимического общества 157 , A903 – A911 (2010).
CAS Статья Google ученый
Левандовски, А.& Świderska-Mocek, A. Ионные жидкости как электролиты для литий-ионных аккумуляторов — обзор электрохимических исследований. Журнал источников энергии 194 , 601–609 (2009).
ADS CAS Статья Google ученый
Сато Т., Маруо Т., Марукане С. и Такаги К. Ионные жидкости, содержащие карбонатный растворитель в качестве электролитов для литий-ионных элементов. Журнал источников энергии 138 , 253–261 (2004).
ADS CAS Статья Google ученый
Чжэн, Х., Цзян, К., Абэ, Т. и Огуми, З. Электрохимическое интеркалирование лития в анод из природного графита в ионных жидких электролитах на основе четвертичного аммония. Углерод 44 , 203–210 (2006).
CAS Статья Google ученый
Плечкова Н.В. и Седдон К.R. Применение ионных жидкостей в химической промышленности. Обзоры химического общества 37 , 123–150 (2008).
CAS PubMed Статья Google ученый
Роджерс Р., Плечкова Н. и Седдон К. В ACS Symposium Series .
Sun, H., Zhang, D., Liu, C. & Zhang, C. Геометрические и электронные структуры дикатона и ионной пары в геминальной дикатионной ионной жидкости 1,3-бис [3-метилимидазолий -ил] пропана бромид. Журнал молекулярной структуры: ТЕОХИМА 900 , 37–43 (2009).
ADS CAS Статья Google ученый
Масри А., Муталиб М. А. и Левек Дж. Обзор дикатионных ионных жидкостей: классификация и применение. Ind. Eng. Управлять. 5 , 1–7 (2016).
Google ученый
Zhang, Z. et al .Асимметричные дикатионные ионные жидкости на основе имидазолия и алифатического аммония в качестве потенциальных электролитных добавок, применяемых для литиевых вторичных батарей. Electrochimica Acta 53 , 4833–4838 (2008).
CAS Статья Google ученый
Широта, Х., Мандаи, Т., Фуказава, Х. и Като, Т. Сравнение дикатионных и монокатионных ионных жидкостей: плотность жидкости, тепловые свойства, поверхностное натяжение и вязкость сдвига. Journal of Chemical & Engineering Data 56 , 2453–2459 (2011).
CAS Статья Google ученый
Ding, Y.-S., Zha, M., Zhang, J. & Wang, S.-S. Синтез, характеристика и свойства геминальных имидазолиевых ионных жидкостей. Коллоиды и поверхности A: физико-химические и технические аспекты 298 , 201–205 (2007).
CAS Статья Google ученый
Хан, А.С. и др. . Дикатионные ионные жидкости на основе имидазолия: синтез и свойства. Журнал молекулярных жидкостей 227 , 98–105 (2017).
CAS Статья Google ученый
Талеби М., Патил Р. А. и Армстронг Д. У. Физико-химические свойства дикатионных ионных жидкостей с разветвленной цепью. Журнал молекулярных жидкостей 256 , 247–255, https: // doi.org / 10.1016 / j.molliq.2018.02.016 (2018).
CAS Статья Google ученый
Tarascon, J. & Guyomard, D. Новые составы электролитов, стабильные в диапазоне напряжений от 0 до 5 В и совместимые с литий-ионными элементами Li1 + xMn2O4 / углерода. Ионика твердого тела 69 , 293–305 (1994).
CAS Статья Google ученый
Sloop, S.Э., Керр, Дж. Б. и Киношита, К. Роль реакционной способности электролита литий-ионного аккумулятора в снижении производительности и саморазряде. Журнал источников питания 119 , 330–337 (2003).
ADS Статья CAS Google ученый
Han, H.-B. и др. . Бис (фторсульфонил) имид лития (LiFSI) как проводящая соль для неводных жидких электролитов литий-ионных аккумуляторов: физико-химические и электрохимические свойства. Журнал источников энергии 196 , 3623–3632 (2011).
ADS CAS Статья Google ученый
Галински М., Левандовски А. и Стэпняк И. Ионные жидкости как электролиты. Electrochimica acta 51 , 5567–5580 (2006).
Артикул CAS Google ученый
Madria, N. et al. .Ионные жидкие электролиты для литиевых батарей: исследования синтеза, электрохимии и цитотоксичности. Журнал источников питания 234 , 277–284 (2013).
CAS Статья Google ученый
Дахби, М., Гамусс, Ф., Тран-Ван, Ф., Лемордант, Д. и Анути, М. Сравнительное исследование электролитов EC / DMC LiTFSI и LiPF6 для электрохимического хранения. Журнал источников энергии 196 , 9743–9750, https: // doi.org / 10.1016 / j.jpowsour.2011.07.071 (2011).
ADS CAS Статья Google ученый
Вассершайд П. и Велтон Т. Ионные жидкости в синтезе . (Джон Вили и сыновья, 2008 г.).
Peljo, P. & Girault, H.H. Окно электрохимического потенциала электролитов батареи: заблуждение HOMO – LUMO. Энергетика и экология 11 , 2306–2309 (2018).
CAS Статья Google ученый
Бард А. Дж. И Фолкнер Л. Р. Основы и приложения. Электрохимические методы 2 , 482 (2001).
Google ученый
Bonhote, P., Dias, A.-P., Papageorgiou, N., Kalyanasundaram, K. & Grätzel, M. Гидрофобные расплавленные соли с высокой проводимостью при температуре окружающей среды. Inorg Chem 35 , 1168–1178 (1996).
CAS PubMed Статья Google ученый
McEwen, A. B., Ngo, H. L., LeCompte, K. & Goldman, J. L. Электрохимические свойства электролитов на основе солей имидазолия для электрохимических конденсаторов. Журнал Электрохимического общества 146 , 1687–1695 (1999).
ADS CAS Статья Google ученый
Макфарлейн, Д., Микин, П., Сан, Дж., Амини, Н. и Форсайт, М. Имиды пирролидиния: новое семейство расплавленных солей и проводящих пластических кристаллических фаз. Журнал физической химии B 103 , 4164–4170 (1999).
CAS Статья Google ученый
Plylahan, N., Kerner, M., Lim, D.-H., Matic, A. & Johansson, P. Ионная жидкость и гибридные ионно-жидкие / органические электролиты для применения в высокотемпературных литий-ионных аккумуляторах . Electrochimica Acta 216 , 24–34 (2016).
CAS Статья Google ученый
Xiong, S. et al. . Роль добавления органических растворителей в ионные жидкие электролиты для литий-серных аккумуляторов. RSC Advances 5 , 2122–2128 (2015).
CAS Статья Google ученый
Фриш, М.J. T. и др. . «Gaussian 09W, Gaussian, Inc.», Wallingford, CT: 2009 (2009).
Жан, К.-Г., Николс, Дж. А. и Диксон, Д. А. Потенциал ионизации, сродство к электрону, электроотрицательность, твердость и энергия электронного возбуждения: свойства молекул из орбитальных энергий теории функционала плотности. Журнал физической химии A 107 , 4184–4195 (2003).
ADS CAS Статья Google ученый
Han, S., Zhang, H., Fan, C., Fan, W. & Yu, L. 1,4-дицианобутан как пленкообразующая добавка для высоковольтных литий-ионных аккумуляторов. Ионика твердого тела 337 , 63–69 (2019).
CAS Статья Google ученый
Zhang, Z. et al. . Фторированные электролиты для литий-ионных аккумуляторов 5 В. Энергетика и экология 6 , 1806–1810 (2013).
CAS Статья Google ученый
Дедривере, Р. и др. . Реакционная способность границы раздела электрод / электролит в высоковольтной шпинели LiMn1. 6Ni0. Литий-ионный аккумулятор 4O4 / Li4Ti5O12. Журнал физической химии C 114 , 10999–11008 (2010).
CAS Статья Google ученый
Pham, H.Q. et al. .Повышение производительности 4,8 В Li1. 2Mn0. 525Ni0. 175Co0. Катод батареи 1O2 с использованием фторированного линейного карбоната в качестве высоковольтной добавки. Журнал Электрохимического общества 161 , A2002 – A2011 (2014).
CAS Статья Google ученый
Леви М. и др. . Твердотельная электрохимическая кинетика интеркаляции Li-Ion в Li1− x CoO2: одновременное применение электроаналитических методов SSCV, PITT и EIS. Журнал Электрохимического общества 146 , 1279–1289 (1999).
ADS CAS Статья Google ученый
Mun, J. et al. . Электрохимическая пассивация поверхности LiCoO 2 с помощью аллилового ионного жидкого электролита для современных, безопасных литий-ионных аккумуляторов. Научные отчеты 4 , 5802 (2014).
CAS PubMed PubMed Central Статья Google ученый
Нара, Х., Мукояма, Д., Симидзу, Р., Момма, Т. и Осака, Т. Систематический анализ межфазного сопротивления между катодным слоем и токоприемником в литий-ионных аккумуляторах с помощью спектроскопии электрохимического импеданса. Журнал источников энергии 409 , 139–147 (2019).
ADS CAS Статья Google ученый
Gaussian 16 Rev. C.01 (Wallingford, CT, 2016).
Беркманс, Г. и др. . Прогноз стоимости современных литий-ионных аккумуляторов для электромобилей до 2030 года. Энергия 10 , 1314 (2017).
Артикул Google ученый
Zhang, Y. et al. . Катодные материалы высокой энергии для литий-ионных аккумуляторов: обзор последних разработок. Наука Китай Технологические науки 58 , 1809–1828 (2015).
ADS CAS Статья Google ученый
Лин, К., Тан, А., Му, Х., Ван, В. и Ван, К. Механизмы старения электродных материалов в литий-ионных батареях для электромобилей. Химический журнал 2015 (2015).
Эбнер М., Чанг Д. В., Гарсия Р. Э. и Вуд В. Анизотропия извилистости в электродах литий-ионных аккумуляторов. Advanced Energy Materials 4 , 1301278 (2014).
Артикул CAS Google ученый
Батареи: электричество посредством химических реакций
Батареи состоят из одного или нескольких электрохимических элементов, в которых накапливается химическая энергия для последующего преобразования в электрическую энергию.Батареи используются во многих повседневных устройствах, таких как сотовые телефоны, портативные компьютеры, часы и автомобили. Батареи состоят по крайней мере из одного электрохимического элемента, который используется для хранения и выработки электроэнергии. Хотя существует множество электрохимических элементов, батареи обычно состоят по крайней мере из одного гальванического элемента. Гальванические элементы также иногда называют гальваническими элементами. Химические реакции и выработка электрической энергии происходят самопроизвольно внутри гальванического элемента, в отличие от реакций электролитических элементов и топливных элементов.
Введение
Именно во время проведения экспериментов с электричеством в 1749 году Бенджамин Франклин впервые ввел термин «батарея» для обозначения связанных конденсаторов. Однако его батарея была не первой батареей, а просто первой, которую так называли. Скорее всего, считается, что багдадские батареи, обнаруженные в 1936 году и возрастом более 2000 лет, были одними из первых в истории батарей, хотя их точное назначение до сих пор обсуждается.
Луиджи Гальвани (в честь которого назван гальванический элемент) впервые описал «животное электричество» в 1780 году, когда он создал электрический ток через лягушку.Хотя в то время он не знал об этом, это была форма батареи. Его современник Алессандро Вольта (в честь которого названы гальваническая ячейка и гальваническая батарея) был убежден, что «животное электричество» исходит не от лягушки, а от чего-то совершенно другого. В 1800 году он произвел первую настоящую батарею: гальваническую батарею.
В 1836 году Джон Фредерик Даниэлл создал ячейку Даниэля, исследуя способы преодоления некоторых проблем, связанных с гальванической батареей Вольта. За этим открытием последовали разработки ячейки Гроув Уильямом Робертом Гроувом в 1844 году; первая аккумуляторная батарея, сделанная из свинцово-кислотных элементов в 1859 году Гастоном Планте; гравитационная ячейка Калло в 1860-х годах; и ячейка Лекланша Жоржа Лекланша в 1866 году.
До этого момента все батареи были мокрыми. Затем в 1887 году Карл Гасснер создал первую сухую батарею, состоящую из угольно-цинкового элемента. Никель-кадмиевый аккумулятор был представлен в 1899 году Вальдмаром Юнгнером вместе с никель-железным аккумулятором. Однако Юнгнеру не удалось запатентовать никель-железную батарею, и в 1903 году Томас Эдисон запатентовал для себя слегка измененную конструкцию.
Главный прорыв произошел в 1955 году, когда Льюис Урри, сотрудник компании, ныне известной как Energizer, представил обычную щелочную батарею.1970-е годы привели к созданию никель-водородных батарей, а 1980-е — к никель-металлогидридным батареям.
Литиевые батареибыли впервые созданы еще в 1912 году, однако самый успешный тип — литий-ионные полимерные батареи, используемые сегодня в большинстве портативных электронных устройств, — не был выпущен до 1996 года.
Гальванические элементы
Гальванические элементы состоят из двух полуэлементных реакций (окисление-восстановление), связанных между собой через полупроницаемую мембрану (обычно соляную ванну) и проволоку (рис. 1).На каждой стороне ячейки находится металл, который действует как электрод. Один из электродов называется катодом, а другой — анодом. Сторона ячейки, содержащая катод, уменьшена, что означает, что она получает электроны и действует как окислитель для анода. Сторона ячейки, содержащая анод, — это место, где происходит окисление, то есть он теряет электроны и действует как восстановитель для катода. Каждый из двух электродов погружен в электролит, соединение, состоящее из ионов.Этот электролит действует как градиент концентрации для обеих сторон полуреакции, облегчая процесс переноса электронов через провод. Это движение электронов производит энергию и используется для питания батареи.
Клетка разделена на две части, потому что химическая реакция происходит самопроизвольно. Если бы реакция происходила без этого разделения, выделялась бы энергия в виде тепла, и батарея не работала бы.
Рисунок 1: Цинк-медный гальванический элемент.Гальванический элемент вырабатывает электричество, необходимое для питания лампочки.
Типы аккумуляторов
Рисунок 2: Первичные и вторичные батареи. Первичные батареи (слева) одноразовые и одноразовые. Вторичные батареи (справа) перезаряжаемые, как этот аккумулятор сотового телефона.
Первичные батареи
Первичные батареи одноразовые и одноразовые. Электрохимические реакции в этих батареях необратимы.Материалы электродов полностью утилизированы и поэтому не могут регенерировать электричество. Первичные батареи часто используются, когда требуются длительные периоды хранения, поскольку они имеют гораздо меньшую скорость разряда, чем вторичные батареи.
Примером использования первичных батарей являются детекторы дыма, фонарики и большинство пультов дистанционного управления.
Вторичные батареи
Вторичные батареи перезаряжаемые. Эти батареи подвергаются электрохимическим реакциям, которые можно легко обратить.Химические реакции, происходящие во вторичных батареях, обратимы, поскольку компоненты, которые вступают в реакцию, не полностью израсходованы. Перезаряжаемые батареи нуждаются в внешнем источнике электроэнергии для зарядки после того, как они израсходовали свою энергию.
Примером использования аккумуляторных батарей являются автомобильные аккумуляторы и портативные электронные устройства.
Типы аккумуляторных элементов
Влажные камеры
Аккумуляторы с жидким электролитом содержат жидкий электролит. Они могут быть как первичными, так и вторичными.Из-за жидкой природы влажных ячеек для разделения анода и катода используются изоляционные листы. Типы влажных клеток включают клетки Даниэля, клетки Лекланша (первоначально использовавшиеся в сухих клетках), клетки Бунзена, клетки Вестона, клетки хромовой кислоты и клетки Гроув. Свинцово-кислотные элементы в автомобильных батареях представляют собой влажные элементы.
Рисунок 3: Свинцово-кислотный аккумулятор в автомобиле.
Сухие камеры
В сухих аккумуляторных батареях свободная жидкость отсутствует.Вместо этого электролит представляет собой пасту, достаточно влажную, чтобы пропускать ток. Это позволяет эксплуатировать сухую батарею в любом положении, не беспокоясь о том, что ее содержимое разольется. Вот почему сухие батареи обычно используются в изделиях, которые часто перемещают и переворачивают, например, в портативных электронных устройствах. Батареи с сухими элементами могут быть как первичными, так и вторичными. Самая распространенная батарея с сухими элементами — это элемент Лекланша.
Производительность батареи
Емкость батареи напрямую зависит от количества материала электрода и электролита внутри элемента.Первичные батареи могут терять от 8% до 20% своего заряда в течение года без какого-либо использования. k} \]
, где I — ток, k — константа около 1.3, t — это время, в течение которого аккумулятор может выдерживать ток, а Q p — это емкость при разряде со скоростью 1 ампер.
Ток, напряжение и стандартный понижающий потенциал
Существует значительная корреляция между током и напряжением ячейки. Ток, как следует из названия, представляет собой поток электрического заряда. Напряжение — это то, сколько тока потенциально может протекать через систему. На рисунке 4 показана разница между током и напряжением.
Рисунок 4: Разница между напряжением и током.
Вода течет из шланга на водяное колесо, вращая его. Ток можно представить как количество воды, протекающей по шлангу. Напряжение можно рассматривать как давление или силу воды, протекающей по шлангу. По первому шлангу не проходит много воды, а также отсутствует давление, и, следовательно, он не может эффективно вращать водяное колесо.По второму шлангу протекает значительное количество воды, поэтому в нем большое количество тока. Через третий шланг протекает не так много воды, но есть что-то, что блокирует большую часть шланга. Это увеличивает давление воды, вытекающей из шланга, придавая ей большое напряжение и позволяя воде ударяться о водяное колесо с большей силой, чем в первом шланге.
Стандартный понижающий потенциал, E o , представляет собой измерение напряжения. Стандартный восстановительный потенциал можно рассчитать, зная, что это разность энергетических потенциалов между катодом и анодом : E o ячейка = E o катод — E o анод .Для стандартных условий электродные потенциалы для полуэлементов могут быть определены с помощью таблицы стандартных электродных потенциалов.
Для нестандартных условий определить электродный потенциал для катода и анода не так просто, как взглянуть на таблицу. Вместо этого необходимо использовать уравнение Нернста для определения E o для каждой половины ячейки. Уравнение Нернста представлено как, где R — универсальная газовая постоянная (8,314 JK — 1 моль, — 1 ), T — температура в Кельвинах, n — количество моль перенесенных электронов. в полуреакции F — постоянная Фарадея (9.648 x 10 4 C моль -1 ), а Q — коэффициент реакции.
Аккумуляторы разных размеров и некоторые дополнительные факты
Батареи различаются по размеру и напряжению в зависимости от химических свойств и содержимого элемента. Однако батареи разных размеров могут иметь одинаковое напряжение. Причина этого явления в том, что стандартный потенциал ячейки зависит не от размера батареи, а от ее внутреннего содержимого. Следовательно, батареи разных размеров могут иметь одинаковое напряжение (Рисунок 5).Кроме того, есть способы, с помощью которых аккумуляторы могут увеличивать свое напряжение и ток. Когда батареи выстраиваются в ряд рядов, это увеличивает их напряжение, а когда батареи выстраиваются в ряд столбцов, это может увеличить их ток.
Рисунок 5: Четыре батареи разного размера, все с напряжением 1,5
Опасности
Батареи могут взорваться в результате неправильного использования или неисправности. При попытке перезарядить аккумулятор или зарядить его с чрезмерной скоростью в аккумуляторе могут накапливаться газы и потенциально вызвать разрыв.Короткое замыкание также может привести к взрыву. Батарея, помещенная в огонь, также может привести к взрыву, поскольку внутри батареи накапливается пар. Утечка также вызывает беспокойство, поскольку химические вещества внутри батарей могут быть опасными и опасными. Утечка, исходящая из батарей, может повредить устройство, в котором они находятся, и с ней опасно обращаться. Широкое использование батарей вызывает множество экологических проблем. Производство аккумуляторов требует много ресурсов и включает обращение со многими опасными химическими веществами.Использованные батареи часто утилизируются ненадлежащим образом и являются электронным мусором. Материалы внутри батарей потенциально могут быть токсичными загрязнителями, что делает неправильную утилизацию особенно опасной. Благодаря программам утилизации электроники токсичные металлы, такие как свинец и ртуть, не попадают в окружающую среду и не наносят ей вреда. Использование батареек опасно и может привести к смерти.
Самодельные батарейки
Любой жидкий или влажный объект, который имеет достаточно ионов, чтобы быть электропроводным, может быть использован для изготовления батареи.Можно даже генерировать небольшое количество электричества, вставляя электроды из разных металлов в картофель, лимоны, бананы или газированную колу. Гальваническую кучу можно создать, используя две монеты и бумагу, смоченную в соленой воде. Сложение нескольких монет в серию может привести к увеличению тока.
Практические задачи
Проблемы
1. Да / Нет
- Будет ли добавление батарей, выстроенных в ряд, увеличивать общее напряжение батарей?
- Происходят ли в электролитических ячейках непроизвольные химические реакции?
- Перезаряжаемые батареи также называют одноразовыми?
- Могут ли батареи разных размеров иметь одинаковое напряжение?
2.Т / Ф
- В первичных ячейках почти всегда полностью используются все компоненты электродов.
- Первичные и вторичные элементы различаются катодными и анодными свойствами.
- Редокс-реакции играют важную роль в элементах батарей.
- Катод в гальванической ячейке получает электроны.
3. Определите стандартный электродный потенциал гальванической ячейки в ячейке Лекланша (сухой) с половинным напряжением ячейки.875 В на графитовом катоде и 0,253 В на цинковом аноде.
4. Определите стандартный потенциал электрода с заданными напряжениями половины ячейки, равными 0,987 В на катоде и 0,632 В на аноде.
5. Объясните, почему аккумуляторные батареи могут быть лучше одноразовых.
Решения
1. Да / Нет
- Есть
- Есть
- №
- Есть
2. Т / Ф
- Истинно
- Ложь
- Истинно
- Истинно
3.E 0 ячейка = E 0 (катод) -E 0 (анод)
E 0 ячейка l = 0,875 В — 0,253 В = 0,622 В
4. E 0 элемент = E 0 (катод) -E 0 (анод)
E 0 ячейка = 0,987 В -0,632 В = 0,355 В
5. Хотя одноразовые батареи изначально дешевле и их проще изготавливать, более длительный срок службы аккумуляторных батарей часто бывает более эффективным и полезным.Перезаряжаемые батареи означают меньше отходов, так как меньше батарей нужно производить и меньше утилизировать на свалках или в рамках программ утилизации. Перезаряжаемые батареи также более удобны, поскольку их замена больше не требуется. Это особенно полезно для портативных электронных устройств. Кроме того, поскольку компоненты вторичного элемента являются многоразовыми, перезаряжаемые батареи обычно будут стоить меньше, чем одноразовые батареи в долгосрочной перспективе.
 Должно пройти некоторое время, чтобы вода хорошо перемешалась с водой. Обычно для этого требуется 3-4 часа;
Должно пройти некоторое время, чтобы вода хорошо перемешалась с водой. Обычно для этого требуется 3-4 часа;



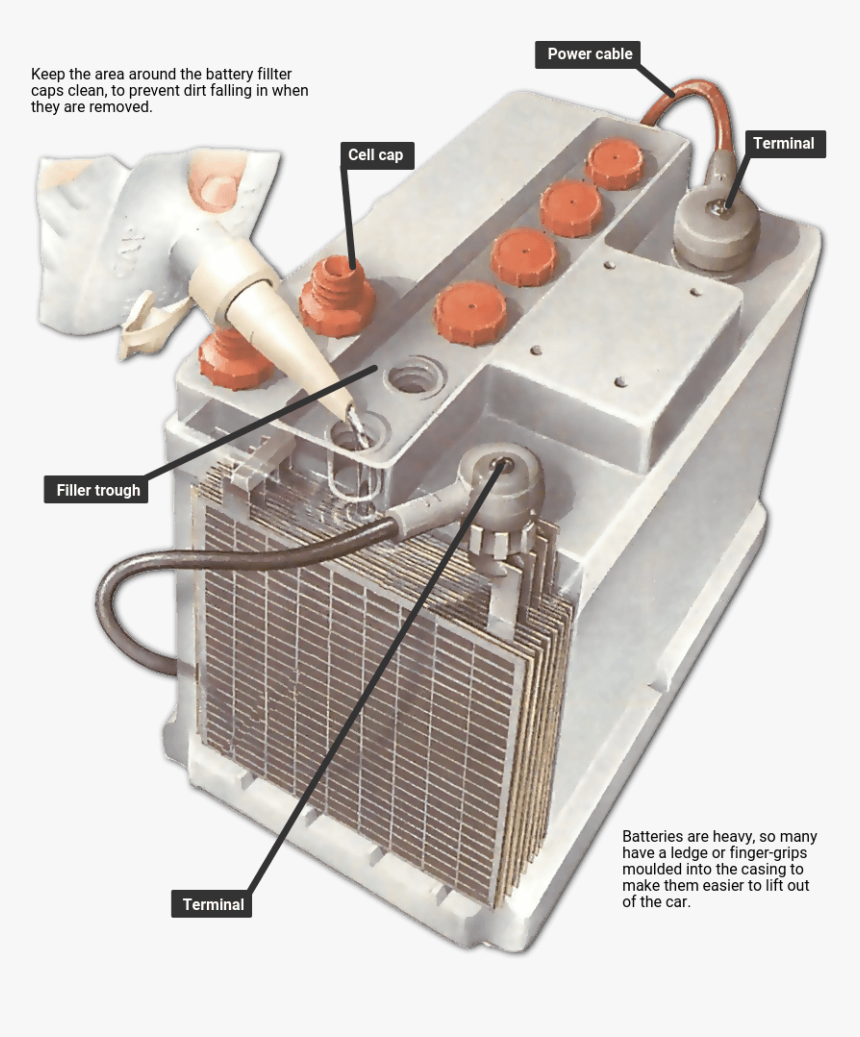
 Если загрязнения довольно сильные, лучше воспользоваться щеткой (неметаллической).
Если загрязнения довольно сильные, лучше воспользоваться щеткой (неметаллической).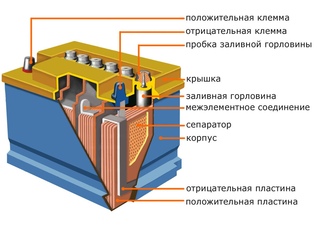
 Системы охлаждения материала с фазовым переходом могут удовлетворить требования к охлаждению аккумуляторной батареи, однако изменение объема, которое происходит во время фазового перехода, ограничивает ее применение.Кроме того, материал с фазовым переходом может только поглощать выделяемое тепло, но не отводить его, что означает, что он не сможет снизить общую температуру, как и другие системы. Хотя материалы с фазовым переходом не подходят для использования в транспортных средствах, они могут быть полезны для улучшения тепловых характеристик в зданиях за счет уменьшения колебаний внутренней температуры и снижения пиковых охлаждающих нагрузок.
Системы охлаждения материала с фазовым переходом могут удовлетворить требования к охлаждению аккумуляторной батареи, однако изменение объема, которое происходит во время фазового перехода, ограничивает ее применение.Кроме того, материал с фазовым переходом может только поглощать выделяемое тепло, но не отводить его, что означает, что он не сможет снизить общую температуру, как и другие системы. Хотя материалы с фазовым переходом не подходят для использования в транспортных средствах, они могут быть полезны для улучшения тепловых характеристик в зданиях за счет уменьшения колебаний внутренней температуры и снижения пиковых охлаждающих нагрузок. Использование ребер нашло большой успех в электронике, и традиционно они использовались в качестве дополнительной системы охлаждения на транспортных средствах с двигателями внутреннего сгорания. Использование ребер для охлаждения аккумулятора электромобиля вышло из употребления, поскольку дополнительный вес ребер перевешивает преимущества охлаждения.
Использование ребер нашло большой успех в электронике, и традиционно они использовались в качестве дополнительной системы охлаждения на транспортных средствах с двигателями внутреннего сгорания. Использование ребер для охлаждения аккумулятора электромобиля вышло из употребления, поскольку дополнительный вес ребер перевешивает преимущества охлаждения.
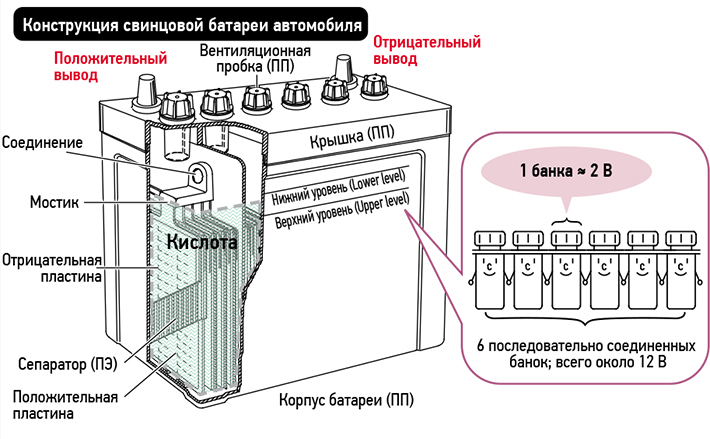 Однако конструкция системы охлаждения электромобилей будет выглядеть иначе. Структура системы охлаждения, которая обеспечивает максимальную однородность температуры, зависит от формы аккумуляторной батареи и будет выглядеть по-разному для каждого производителя автомобиля.
Однако конструкция системы охлаждения электромобилей будет выглядеть иначе. Структура системы охлаждения, которая обеспечивает максимальную однородность температуры, зависит от формы аккумуляторной батареи и будет выглядеть по-разному для каждого производителя автомобиля.